TØ 17 – Lipider og cellemembraner
1 Opgave 1. Membransammensætning
1.1 Sammenlign membransmeltetemperaturer
For to membransystemer, hvor den ene er sammensat af phospholipider med mættede acylkæder på 20 kulstofatomer og den anden af kæder af samme længde men med cis-dobbeltbindinger på både C-5, C-8, C-11 og C-14, hvilke forskelle i smeltetemperatur vil du så forvente?
Bakterier med visse mutationer er ikke i stand til at syntetisere fedtsyrer og inkorporerer derfor fedtsyrer fra mediet i deres membraner.
1.2 Forudsig fedtsyresammensætning ved temperatur
Antag at du har to kulturer, der hver indeholder en blanding af forskellige typer lige-kædede fedtsyrer, nogle mættede og andre umættede og med varierende kædelængde fra 10-20 kulstofatomer. Hvis den ene kultur fastholdes ved 18°C og den anden ved 40°C over flere generationer, hvilke forskelle vil du så forvente at opleve i sammensætningen af de to kulturers cellemembraner?
1.3 Sammenlign hopanoider og kolesterol
Hopanoider er pentacykliske molekyler, der findes i bakterier og visse planter. En typisk hopanoidstruktur er vist nedenfor. Sammenlign strukturen med kolesterol.
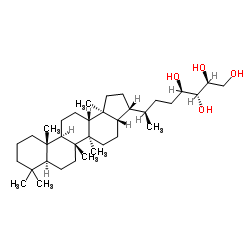
1.4 Forudsig hopanoidernes membraneffekt
Hvilken effekt vil du forvente at hopanoid har på den bakterielle cellemembran?
2 Opgave 2. Helical wheel
Membranspændende helicer består typisk af 18 to 20 aminosyrer.
2.1 Beregn hydrofob membranbredde
Beregn bredden af den hydrofobe del af cellemembranen baseret på dette.
2.2 Fortolk helical wheel-plot
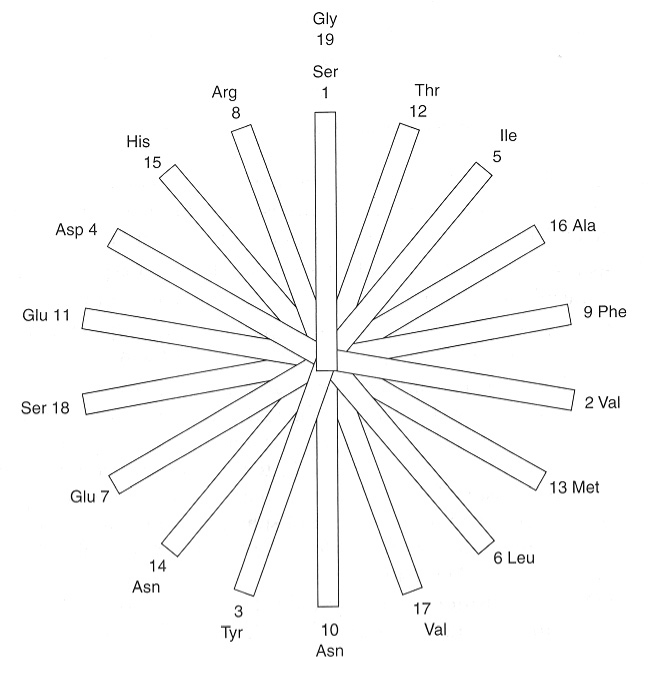
Sekvensen af sådan en helix kan plottes i et såkaldt helical wheel, der viser positionen af hver aminosyrerest rundt om helicens akse.
Forklar hvilke egenskaber ved transmembrane helicer, der kan forudsiges på baggrund af et helical wheel-plot.
2.3 Analysér amfipatisk helix
I eksemplet nedenfor, analysér positionen af de hydrofobe og hydrofile aminosyrerester. Hvordan stabiliseres de hydrofile sidekæder inde i membranen?
Ser-Val-Tyr-Asp-Ile-Leu-Glu-Arg-Phe-Asn-Glu-Thr-Met-Asn-His-Ala-Val-Ser-Gly2.4 Vis prostaglandins ligander i PyMOL
Lav en scene, kaldet F1, der viser prostaglandin (PDB-ID: 1PTH). Hvilke ligander er bundet? Hvilke tror I findes i den native struktur og hvilke er produkt af krystalliseringsmetoden?
2.5 Analysér elektrostatisk membranlokalisering
Analyser den elektrostatiske overflade af prostaglandin. Lav en scene, kaldet F2, der viser dette. Hvordan er prostaglandin lokaliseret til membranen - forklar ud fra det beregnede elektrostatiske potentiale?
2.6 Analysér TM-helicernes elektrostatik
Kig nærmere på alphahelicerne mellem rest 74 og 124 og undersøg deres elektrostatiske overflade. Hint: Lav alphahelicerne et objekt. Analyser de enkelte helicers ligesom I gjorde med helix-wheel plottet. Stemmer det overens med det forventede?
3 Opgave 3. Hydropatiplot
3.1 Analyser hydropatiplot
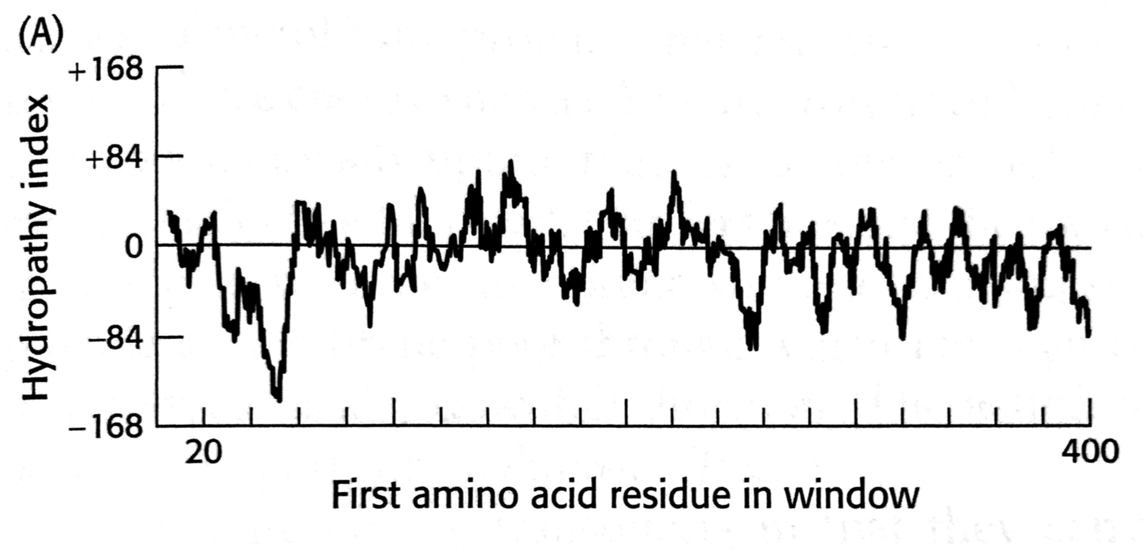
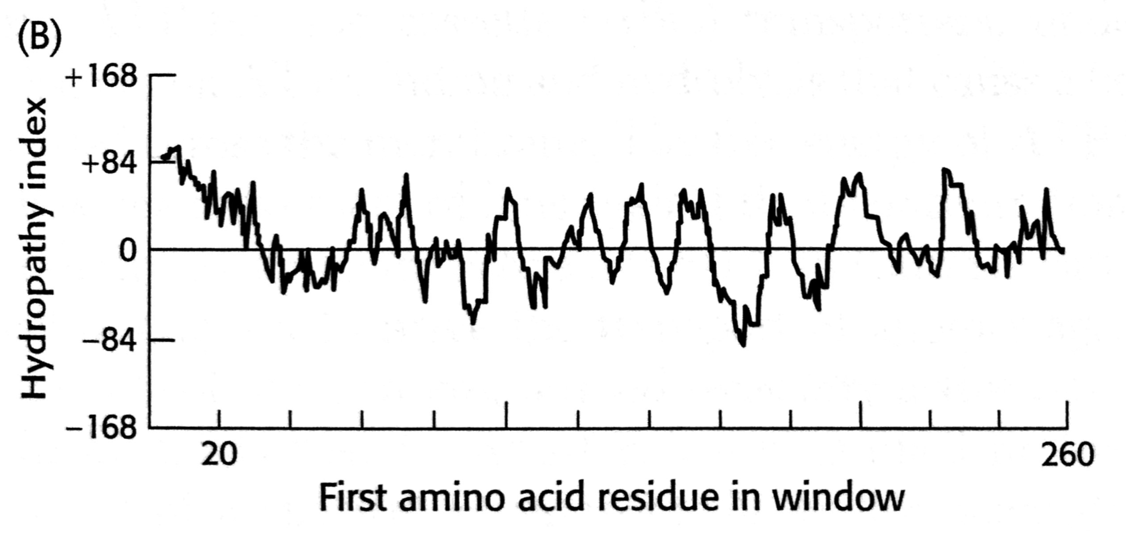
Analysér nedenstående hydropatiplot for tilstedeværelse af transmembrane segmenter:
3.2 Vurdér analysens usikkerheder
Hvilke usikkerheder ligger der i analysen?
4 Opgave 4. Breast Cancer Resistance Protein (BCRP)
Kvinder med brystkræft udvikler af og til resistens mod et bredt spektrum af cytotoxiske medikamenter brugt i kemoterapien. Baggrunden for dette synes at ligge i en opregulering af ekspression af en række multidrug-resistance proteiner tilhørende gruppen af membranassocierede ABC-transportere. BCRP er en sådan transporter, hvis aminosyresekvens udledt fra cDNA er vist nedenfor.
1 20 40 60
MSSSNVEVFI PVSQGNTNGF PATASNDLKA FTEGAVLSFH NICYRVKLKS GFLPCRKPVE
80 100 120
KEILSNINGI MKPGLNAILG PTGGGKSSLL DVLAARKDPS GLSGDVLING APRPANFKCN
140 160 180
SGYVVQDDVV MGTLTVRENL QFSAALRLAT TMTNHEKNER INRVIQELGL DKVADSKVGT
200 220 240
QFIRGVSGGE RKRTSIGMEL ITDPSILFLD EPTTGLDSST ANAVLLLLKR MSKQGRTIIF
260 280 300
SIHQPRYSIF KLFDSLTLLA SGRLMFHGPA QEALGYFESA GYHCEAYNNP ADFFLDIING
320 340 360
DSTAVALNRE EDFKATEIIE PSKQDKPLIE KLAEIYVNAS FYKETKAELH QLSGGEKKKK
380 400 420
ITVFKEISYT TSFCHQLRWV SKRSFKNLLG NPQASIAQII VTVVLGLVIG AIYFGLKNDS
440 460 480
TGIQNRAGVL FFLTTNQCFS VVSAVELFVV EKKLFIHEYI SGYYRVSSYF LGKLLSDLLP
500 520 540
MRMLPSIIFT CIVYFMLGLK PKADAFFVMM FTLMMVAYSA SSMALAIAAG QSVVSVATLL
560 580 600
MTICFVFMMI FSGLLVNLTT IASWLSWLQY FSIPRYGFTA LQHNEFLGQN FCPGLNATGN
620 640
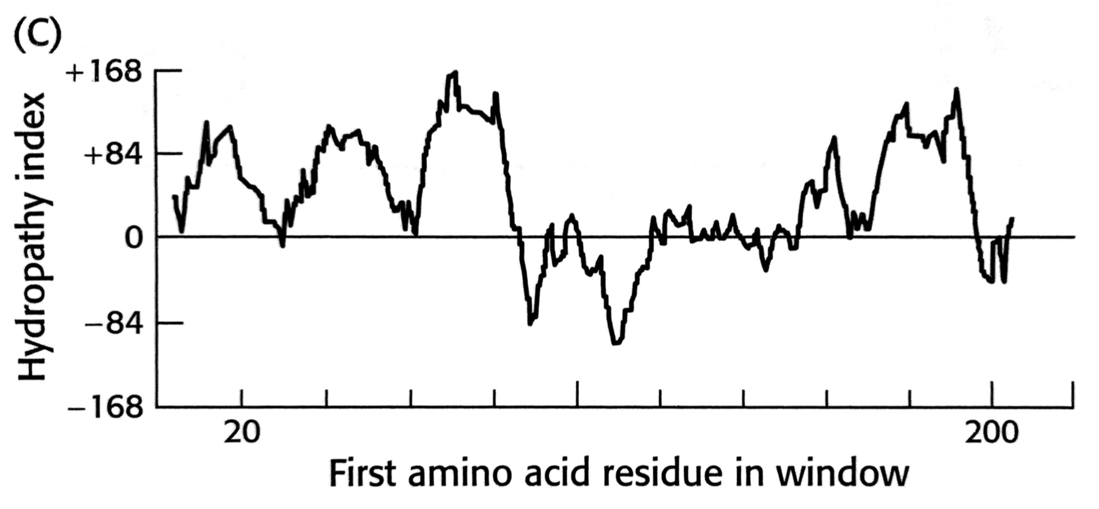
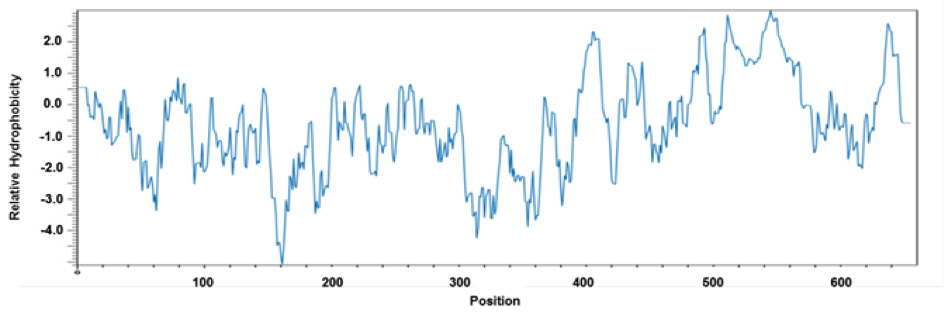
NPCNYATCTG EEYLVKQGID LSPWGLWKNH VALACMIVIF LTIAYLKLLF LKKYSHydrofobicitetsanalyse af BCRP giver desuden følgende resultat:
4.1 Identificér TM-helicer i BCRP-hydropatiplot
Hvilke egenskaber af hydropatiplottet understøtter idéen om at BCRP indeholder transmembrane helicer?
4.2 Anslå antal og placering af TM-helicer
Anslå antallet og den omtrentlige placering af de transmembrane helicer i BCRP.
4.3 Find ATP-bindende kassette i sekvens
ABC-transportere indeholder en såkaldt ATP-bindende kassette og benytter energien fra ATP til selve eksportprocessen.
Foreslå hvilken del af sekvensen ovenfor, der indeholder den ATP-bindende kassette.
4.4 Tegn BCRP-topologi i membran
For at forstå foldningen af membranproteinet indsatte man et peptid med sekvensen YPYDVPDYA på 12 forskellige positioner i BCRP-sekvensen. De resulterende konstrukter (samt vildtype BCRP og en negativ kontrol) blev herefter transfekteret i epithelceller og analyseret for evnen til at binde et radioaktivt mærket antistof rejst mod YPYDVPDYA-sekvensen. Resultatet af analysen er vist i tabellen nedenfor.
| Konstrukt | Substitution (position fra-til) |
Radioaktiv mærkning |
|---|---|---|
| vildtype | - | |
| negativ kontrol | - | |
| N-term | 2 - 10 | - |
| 1 | 405 - 413 | - |
| 2 | 416 - 424 | ++ |
| 3 | 450 - 458 | - |
| 4 | 455 - 463 | - |
| 5 | 475 - 483 | - |
| 6 | 485 - 493 | - |
| 7 | 498 - 506 | + |
| 8 | 540 - 548 | - |
| 9 | 570 - 578 | ++ |
| 10 | 635 - 643 | - |
| C-term | 655 - 663 | - |
Topologisk analyse af BCRP. ++ stærk, + medium og – ingen mærkning.
Lav en skitse af BCRP som det er indlejret i cellemembranen. Er N- og C-terminalerne placeret på samme eller modsatte side af membranen?
4.5 Angiv mulige N-glykosyleringssites
Angiv mulige N-glykosyleringssites i sekvensen for BCRP.
4.6 Fortolk glykosyleringsanalysen
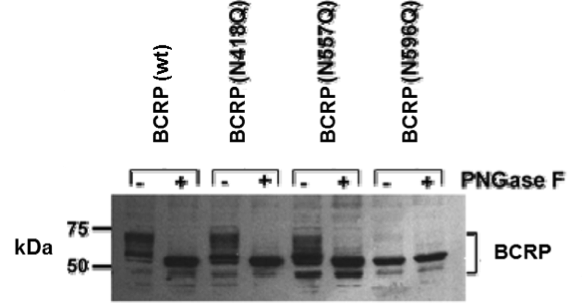
For at undersøge om BCRP er glykosyleret, muterede man desuden specifikke asparaginrester. Proteinekstrakter fra celler transfekteret med mutant BCRP blev derefter analyseret ved SDS-PAGE før og efter behandling med PNGase F. Resultatet af analysen vises nedenfor.
Hvad fortæller analysen om glycosyleringerne i BCRP? Begrund dit svar.
5 Opgave 5. 5’-Nucleotidase
Enzymet 5’-nucleotidase (5’-ribonucleotide phosphohydrolase) er et glycoprotein, der findes associeret med plasmamembranen i mange celler. Enzymet kan forholdsvis let isoleres fra placenta ved brug af detergenter og har en masse på 71 kDa som bedømt med SDS-PAGE.
5.1 Beskriv 5’-nucleotidasens reaktion
Hvilken type reaktion antyder navnet at 5’-nucleotidase udfører?
5.2 Forklar detergentens rolle i oprensning
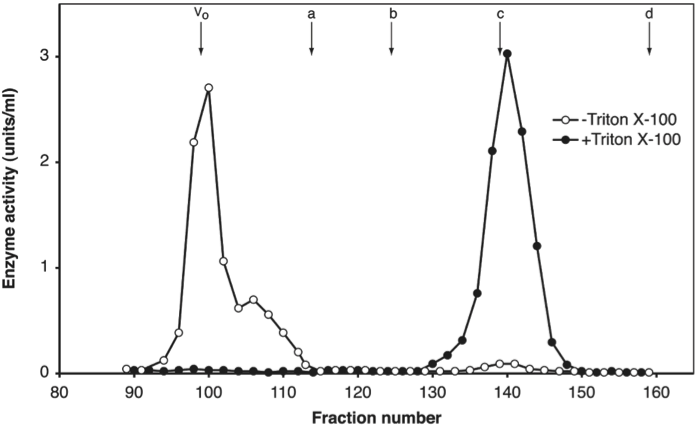
Ved gelfiltrering af det ekstraherede enzym på Sephacryl S-300-søjle under tilstedeværelse af 0.1% Triton X-100 (en detergent), eluerer enzymet svarende til et 150 kDa protein. Uden detergent eluerer enzymet i void-volumen som vist nedenfor.
Beskriv den rolle, detergenten spiller i oprensningen.
5.3 Bestem kvarternær struktur
Hvad er den mest sandsynlige kvarternære struktur af enzymet, når det er bundet til cellemembranen?
5.4 Forklar interfaselokalisering
Aminosyresekvensen af human placental 5’-nukleotidase afledt fra cDNA er vist nedenfor. Enzymet syntetiseres med et signalpeptid på 26 rester samt et stærkt hydrofobt område umiddelbart før stopkodon.
1 30 60
MCPRAARAPA TLLLALGAVL WPAAGAWELT ILHTNDVHSR LEQTSEDSSK CVNASRCMGG
90 120
VARLFTKVQQ IRRAEPNVLL LDAGDQYQGT IWFTVYKGAE VAHFMNALRY DAMALGNHEF
150 180
DNGVEGLIEP LLKEAKFPIL SANIKAKGPL ASQISGLYLP YKVLPVGDEV VGIVGYTSKE
210 240
TPFLSNPGTN LVFEDEITAL QPEVDKLKTL NVNKIIALGH SGFEMDKLIA QKVRGVDVVV
270 300
GGHSNTFLYT GNPPSKEVPA GKYPFIVTSD DGRKVPVVQA YAFGKYLGYL KIEFDERGNV
330 360
ISSHGNPILL NSSIPEDPSI KADINKWRIK LDNYSTQELG KTIVYLDGSS QSCRFRECNM
390 420
GNLICDAMIN NNLRHTDEMF WNHVSMCILN GGGIRSPIDE RNNGTITWEN LAAVLPFGGT
450 480
FDLVQLKGST LKKAFEHSVH RYGQSTGEFL QVGGIHVVYD LSRKPGDRVV KLDVLCTKCR
510 540
VPSYDPLKMD EVYKVILPNF LANGGDGFQM IKDELLRHDS GDQDINVVST YISKMKVIYP
570
AVEGRIKFST GSHCHGSFSL IFLSLWAVIF VLYQFor at forstå enzymets associering med membranen blev det oprensede protein opløst i 45% myresyre og nedbrudt med CNBr i 20 timer, hvorefter reaktionsblandingen blev udrystet med hexan. Efter centrifugering observerede man tre lag, øverst et lag bestående af hexan, i bunden et lag af vandig myresyre og i interfasen mellem disse, et tyndt ugennemsigtigt lag. Dette tynde lag viste sig at indeholde et 3 kDa fragment, der efterfølgende blev behandlet med en endopeptidase specifik for lysinrester. Efter endnu en hexanekstraktion kunne man isolere et dipeptid fra interfasen.
Hvorfor findes 3 kDa-fragmentet og dipeptidet i interfasen mellem hexanfasen og den vandige fase?
5.5 Lokalisér fragmenter i sekvensen
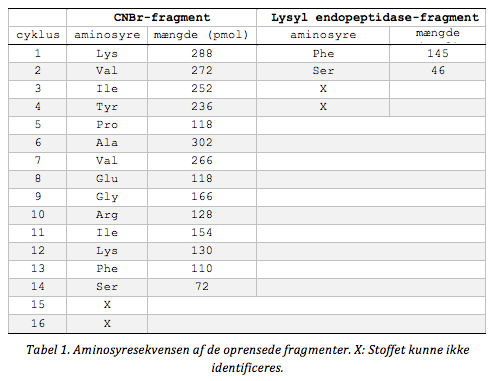
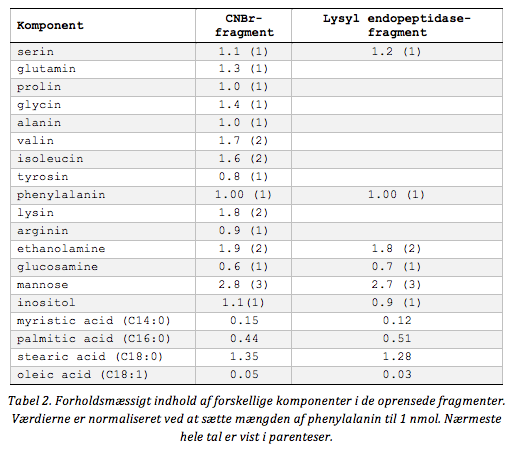
Aminosyresekvensen af CNBr-fragmentet og dipeptidet kan ses i Tabel 1 nedenfor mens sammensætningen af fragmenterne er vist i Tabel 2. Begge fragmenter indeholder et komplekst glykolipid og udover komponenterne listet i tabellerne indeholder fragmenterne også glycerol og phosphat. Glykosamine var desuden på formen N-acetyl glukosamine.
Lokalisér 3 kDa-fragmentet og dipeptidet i aminosyresekvensen. Hvilken rest udgør C-terminalen i det modne enzym?
### Find glykolipid-bindingsrest
Hvilken aminosyrerest er kovalent bundet til glykolipidet?
### Identificér GPI-membrananker
Enzymet kan frigøres fra membranen ved behandling med en inositolspecifik phospholipase C. Hvordan kunne man forestille sig at det er forankret til membranen?
### Beskriv GPI-ankermodifikation
Foreslå hvordan det hydrofobe område nær C-terminalen kan være involveret modifikation af enzymet. Hvor i cellen finder denne modifikation sted?
### Bestem enzymets membranlokalisering
På hvilken side af plasmamembranen er 5’-nucleotidase lokaliseret? Diskutér mulige, biologiske roller for enzymet.