TØ 2 – Introduktion til TØ
I dette TØ sæt arbejdes der på at blive introduceret til TØ formatet med gruppearbejde og præsentation af løsning på opgaver. Opgaverne drejer sig mest om repetition af viden fra tidligere kurser (Berg kapitel 1, 2 og 5) samt anvendelse af PyMOL til analyse af enzym struktur og Excel til analyse af enzym funktion.
1 Opgave 1. Buffer-beregninger
Denne opgave er repetition af Berg Biochemistry kapitel 1.
En forsker forbereder en buffer af eddikesyre og natriumacetat med en pH-værdi på 5,0. Den samlede koncentration af begge komponenter i bufferen er 250 mM, og eddikesyre har en pKa-værdi på 4,75.
1.1 Beregn bufferkomponenternes koncentrationer
Hvad er koncentrationerne af eddikesyre og natriumacetat i bufferen?
1.2 Beregn molmængder i bufferen
Hvor mange mol eddikesyre og natriumacetat er der i 2 L af bufferen?
1.3 Beregn gram af komponenterne
Hvor mange gram eddikesyre og natriumacetat er der i 2 L af bufferen?
Den molære masse af eddikesyre er 60,05 g/mol; den molære masse af natriumacetat er 82,03 g/mol.
2 Opgave 2. Aminosyrers pKa
Denne opgave er repetition af Berg Biochemistry kapitel 2.
2.1 Identificer ioniserbare aminosyresidekæder
Hvilke aminosyresidekæder kan almindeligvis fraspalte eller optage en proton under biologiske forhold og hvad er deres pKa-værdier?
2.2 Bestem sidekædeladning over og under pKa
Hvad er ladningen af en aminosyres sidekæde ved pH-værdier hhv. under og over denne pKa?
2.3 Diskuter variation af aminosyre pKa
Er en aminosyres pKa altid den samme? Hvis ikke, i hvilke situationer kan pKa ændres?
3 Opgave 3. Glutathione
Denne opgave er repetition af Berg Biochemistry kapitel 2.
Glutathione (GSH) er en antioxidant i planter, dyr, svampe og visse bakterier og archaea. Glutathione forhindrer skade på vigtige, cellulære komponenter som følge af reaktive oxygen-forbindelser som frie radikaler, peroxider og tungmetaller.
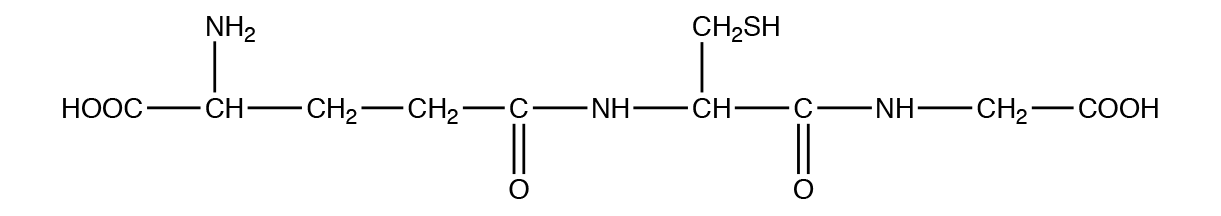
Glutathion har følgende struktur:
Hvilke af følgende udsagn om molekylet er korrekte?
3.1 Vurder tilstedeværelse af α-aminogruppe
Det indeholder en \(\alpha\)-aminogruppe.
3.2 Vurder atypisk peptidbinding
Der findes en kobling mellem to aminosyrer, der adskiller sig fra den almindelige peptidbinding.
3.3 Vurder let oxidérbar gruppe
Der findes en let oxidérbar gruppe.
3.4 Vurder tilstedeværelse af sekundær aminogruppe
Der findes to sekundære aminogrupper.
3.5 Vurder alternativ nomenklatur
Man kunne også beskrive stoffet som Glu-Cys-Gly.
Bemærk at der kan være mere end ét rigtigt svar. Argumentér for hvert af de 5 tilfælde, både dem, du mener er korrekte og dem, du mener er forkerte.
4 Opgave 4. Bereging af enzymkinetik
Denne opgave er repetition af Berg Biochemistry kapitel 5.
Hydrolysen af pyrofosfat til orthofosfat driver biosyntetiske reaktioner såsom DNA-syntese. Denne hydrolytiske reaktion katalyseres i E. coli af en pyrofosfatase, der har en masse på 120 kDa og består af seks identiske underenheder. For dette enzym defineres en aktivitetsenhed som den mængde enzym, der hydrolyserer 10 μmol pyrofosfat på 15 minutter ved 37 °C under standard assaybetingelser. Det oprensede enzym har et 𝑉max på 2800 enheder pr. milligram enzym.
4.1 Beregn \(V_\mathrm{max}\) i mikromol per sekund
Hvor mange mikromol substrat hydrolyseres pr. sekund pr. milligram enzym, når substratkoncentrationen er meget større end \(K_M\)? Med andre ord, hvad er \(V_\mathrm{max}\) for den katalyserede reaktion? Angiv mængde hydrolyseret substrat i μmol.
4.2 Beregn antal active sites per milligram
Hvor mange mikromol active sites er der i 1 mg enzym? Antag, at hver underenhed har ét active site. Angives i μmol.
4.3 Beregn enzymets omsætningstal
Hvad er enzymets omsætningstal i \(s^{-1}\)?
5 Opgave 5. Analyse af Chymotrypsin i PyMOL
I denne opgave skal vi bruge PyMOL til at kigge på strukturen af chymotrypsin, som beskrives på s. 223-226 i Berg Biochemistry 10. udgave. Åbn filen chymotrypsin.pse, pse-filer er PyMOL session filer, som du kan dobbeltklikke på for at åbne filen i PyMOL såfremt programmet er installeret.
5.1 Lokalisér β-barrel domænerne
Chymotrypsin består af to β-barrels kaldet domæne 1 og 2 vist med henholdsvis blåt og rødt. Lokalisér de to domæner og prøv at tænde og slukke for dem med knapperne Domain 1 og Domain 2 i listen til højre. Hvad karakteriserer en β-barrel?
5.2 Undersøg den katalytiske triade
Den katalytiske triade bestående af Ser195, His57 og Asp102 befinder sig i området mellem de to domæner og er vist med grønne streger (sticks) i objektet Triad. Tryk F2 for at se disse aminosyrer tæt på. Hvilken rolle spiller disse for enzymet? Prøv også at identificere andre elementer i strukturen ved at tænde og slukke for dem.
5.3 Forklar pseudo-2-talssymmetri
De to domæner ligner meget hinanden og er arrangeret med en såkaldt pseudo-2-talssymmetri. Tryk F1 på keyboardet for at se ned langs denne akse og F3 og F4 for at se ned langs hvert domæne. Hvad tror du en pseudo-2-talssymmetri er?
5.4 Find aktiveringsskæringen ved residue 16
Når chymotrypsinogen aktiveres til chymotrypsin så bliver molekylet kløvet to steder for at producere kæderne, der her hedder A, B og C (se figur 7.17, s. 224 i Berg Biochemistry 10. udgave). Stykket, der forsvinder mellem kæde B og C er vist med prikker i strukturen (Loop) og er ikke så vigtigt for aktivering. Derimod er skæringen ved residue 16 kritisk. Find residue 16 og forklar hvorfor denne aminosyre er vigtig for aktivering af chymotrypsin.
OBS: Mac-brugere skal holde fn-tasten nede når de trykker på F1, F2, F3 osv, da disse taster også bruges til at styre skærmens lysstyrke etc. på MacBooks.