TØ 6 – Nukleinsyrestruktur 1
1 Opgave 1. Kærlighed ved første blik
🧬 Download DNA-groove-colorblind.pml
I denne opgave skal I lære hvordan proteiner genkender DNA (eller omvendt) for at kunne indgå i en specifik (“romantisk”) binding til hinanden. Hemmeligheden bag denne genkendelse kan findes i Liljas “Textbook of Structural Biology” afsnit 10.2, hvor den specifikke interaktion mellem aminosyrer og DNA-baser beskrives. Aminosyrerne kan genkende både major og minor groove via den såkaldte “groove code”, der er vist i Liljas figur 10.18. Som det ses i figuren herunder er der eksponerede H-bindings-donorer og acceptorer i både major og minor groove og det er disse, som aminosyrerne kan genkende og binde til:
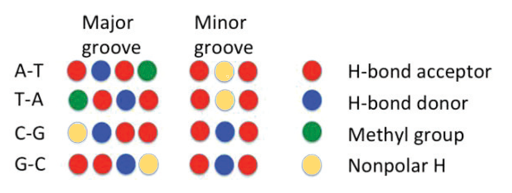
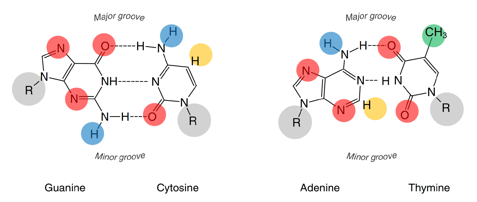
1.1 Forklar specificitet i major groove
Forklar hvorfor der er mere specificitet i binding til major groove end til minor groove.
1.2 Identificer aminosyrer til sekvensspecifik genkendelse
Hvilke aminosyrer vil du tro ofte bruges til sekvensspecifik genkendelse og hvorfor?
1.3 Undersøg groove-mønster for 1BNA
Groove-koden kan være lidt svært at få øje på når man analyserer en DNA dobbelthelix i PyMOL, men med den rette repræsentation bliver den mere tydelig: DNA-groove.pml scriptet, som findes under denne uge på Brightspace, viser DNA-dobbelthelixen som en kuglemodel (spheres), hvor H-bindingsacceptorer er farvet røde, H-bindingsdonorer blå, metylgrupper grønne og ikke-polære hydrogenatomer gule.
PyMOL info: Sphere-repræsentationen viser Van der Waals-radius af atomer og giver dermed et billede af molekylets realistiske form og fylde. Farvning af atomerne ses tydeligere pga. deres størrelse. Til gengæld er det ikke let at aflæse den kemisk sammensætning (som man ser det med sticks) eller den sekundære struktur (som man ser det med cartoon).
Åben DNA dobbelthelix med PDB-ID: 1BNA i PyMOL og fjern vand-molekyler med PyMOL kommandoen “remove solvent”. Brug nu DNA-groove.pml script til at ændre på repræsentationen og farvelægge donorer- og acceptorer i grooves. Rotér molekylet, så du ser ned i major groove (så symmetrien bliver tydelig).
Hvad er specielt ved groove-kode-mønstret for denne DNA dobbelthelix?
2 Opgave 2. Der skal to til tango
Det er vigtigt for DNA-bindende proteiner at kunne gribe fat om DNA-dobbelthelixen og interagere med specifikke base-sekvenser. DNA-molekylet bindes ofte af homodimeriske DNA-bindende proteiner i områder med såkaldte “basepar-palindromer”.
2.1 Giv eksempel på et basepar-palindrom
Giv et eksempel på et “basepar-palindrom” og forklar hvilke geometriske egenskaber det har og hvorfor homodimeriske proteiner kan lide at binde der.
2.2 Beskriv DNA-bindingsdomæner
Som det ses i Tabel 10.1 i Liljas “Textbook of Structural Biology” findes der flere forskellige familier/typer af DNA-bindende proteiner, der via forskellige DNA-bindingsdomæner interagerer med DNA dobbelthelixen.
Beskriv hovedtyperne af DNA-bindingsdomæner og hvordan de interagerer med DNA.
2.3 Diskuter fordele ved heterodimer-binding
DNA-bindende proteiner har en vigtig rolle som gen-specifikke transskriptionsfaktorer, der kan aktivere eller hæmme mRNA syntese. I eukaryoter findes der flere heterodimeriske transkriptionsfaktorer.
Hvad er de mulige fordele ved DNA-binding af en heterodimer?
2.4 Beskriv ligand-binding regulering af DNA
Binding af en ligand til et DNA-bindende protein kan regulere DNA-bindingen.
Hvad er mekanismen hvormed ligand-binding kan påvirke proteinets evne til at binde DNA? Nævn et par eksempler på regulering med denne mekanisme.
3 Opgave 3. TATA-box
Det TATA-box bindende protein (TBP) er involveret i promoter-genkendelse mht. at starte RNA polymerase transskription. TATA-boksen er en 8-basepar del af promoteren, der normalt er lokaliseret 30 nukleotider før transskription start site (TSS). Konsensus-sekvensen er TATA(A/T)A(A/T)(G/A).
Åben TATA.pml scriptet i PyMOL. F1 viser bindingen af TBP langs den heliske akse for DNA-dobbelthelix.
3.1 Find TBP-bindingsgroove
I hvilken groove af DNA-dobbelthelix binder TBP?
Groove kan identificeres ved at zoome ind på basepar og identificere Högsteen- og sukker-side. Vis f.eks. et basepar med kommandoen show sticks, resi 7+23 og zoom ind for at undersøge dette med kommandoerne zoom resi 7+23 og juster dybden med musehjulet, så der fokuseres på baseparret. Rotér derefter så du ser baseparret fra siden. Tryk F2 for at vise den ønskede visning.*
3.2 Beskriv groove-mønstret ved TBP-bindingssted
Tryk F1 og brug groove-kode scriptet (DNA-groove.pml) til at vise DNA-dobbelthelixen som kuglemodel, hvor H-bindingsacceptorer er farvet røde, H-bindingsdonorer blå, metylgrupper grønne og ikke-polære hydrogenatomer gule. Skjul TBP for bedre at kunne se groove-mønster.
Hvad karakteriserer mønsteret i groove, hvor TBP binder?
3.3 Beskriv TBPs sekundære DNA-bindingsstruktur
Hvad karakteriserer TBPs sekundære struktur, der binder til DNA groove?
3.4 Undersøg phenylalanin-interkalering
Tryk F3/F4 for at se et vigtigt element i DNA-protein bindingen, hvor to phenylalaniner interkalerer mellem to basepar.
Hvordan er de to basepar påvirket af interaktionen med de to phenylalaniner? Hvilken standardparameter for den relative orientation af baser (Textbook of Structural Biology, figur 5.16) beskriver bedst konformationen af disse to basepar?
4 Opgave 4. Mad-Max
Max-Myc-Mad er et heterodimerisk transkriptionsfaktor system, der binder specifikt til DNA segmentet CACGTG som tre forskellige komplekser: Myc-Max, Max-Max og Mad-Max. Ifølge forfatterne til den oprindelige artikel om Max-Myc-Mad systemet har navngivningen af Mad (det andet protein i Mad-Max heterodimer) ikke noget at gøre med filmen af samme navn (Youtube link), men kommer fra forkortelsen af “Max dimerization”. Hent PyMOL-scriptet Mad-Max.pml og kør det i PyMOL. Tryk F1 for at se Myc-Max komplekset, tryk F2 for at se Max-Max komplekset, og F3 for at se Mad-Max komplekset.
4.1 Beskriv dimeriseringsdomænet
Beskriv sammensætningen af dimeriseringsdomænet og hvilken egenskab α-helicerne, der binder DNA, har.
4.2 Find bindingsgroove for de tre komplekser
I hvilken groove binder Myc-Max, Max-Max og Mad-Max?
4.3 Beskriv mønster af H-bindings-donor-acceptorer
Orientér molekylet i PyMOL, så du ser ned langs pseudosymmetri aksen af Myc-Max og gem derefter Myc-Max, så kun DNA-dobbelthelixen er synlig. Brug groove-kode scriptet (DNA-groove.pml) til at vise helixgroove-mønsteret.
Hvad er karakteristisk ved mønsteret af H-bindings-donor og -acceptorer?
4.4 Beskriv hydrogenbindinger for aminosyrerne
Tryk F4 for at se hvordan genkendelses-helixer i Myc-Max interagerer med DNA segmentet.
Tryk F5 for at se hvordan genkendelses-helixer i Max-Max interagerer med DNA segmentet.
Tryk F6 for at se hvordan genkendelses-helixer i Mad-Max interagerer med DNA segmentet.
Beskriv hydrogen-bindingerne for de tre aminosyrer (His, Glu, Arg) i genkendelses-helixer i Myc-Max ved at specificere hvilke baser og hvilke atomer på baserne, der indgår i bindingen. Er der andre interaktioner end med baserne? Er interaktionerne symmetriske i Myc-Max, Max-Max og Mad-Max og hvorfor?
Brug menuen “Mouse > Selection mode > Atoms”, så du bedre kan identificere de individuelle atomer, der indgår i hydrogen-bindingerne.*
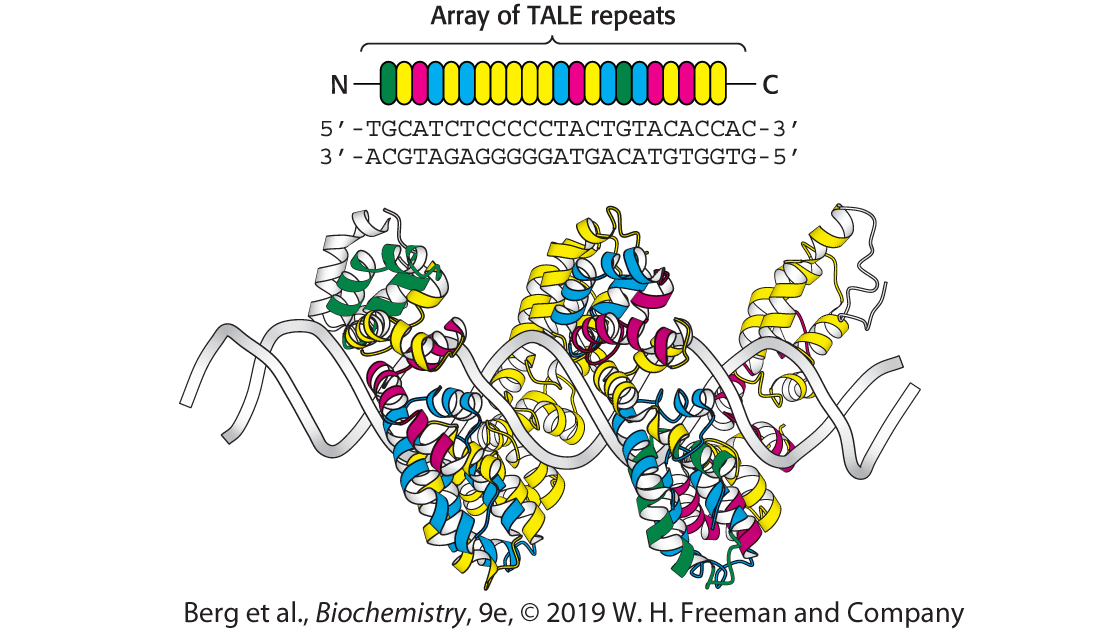
5 Opgave 5. At TALE med DNA
Transskriptionsfaktor-lignende effector nukleaser (TALENs) binder specifikke DNA-sekvenser vha. en række DNA-bindende domæner kaldet TALE-repeats. TALEN-proteiner kan designes til at genkende og kløve specifikke DNA-sekvenser og kan dermed anvendes til genom-redigering (genome editing). TALE-proteiner er omtalt i Berg Biochemistry, udgave 10, side 292, og opbygningen kan ses i figur 9.37 (se nedenstående figur).
5.1 Find TALE-proteinets bindingsgroove
Download og åben scriptet TALE.pml i PyMOL. Tryk F1 og F2 for at se DNA-protein komplekset hhv. fra siden og langs helix aksen. Tryk F3 for at se sphere-repræsentation, hvor man lettere kan se repeat-strukturen. Tryk F4 for at se en specifik interaktion mellem protein og DNA.
I hvilken groove af DNA-dobbelthelixen binder TALE-proteinet? Forklar hvordan du observerer dette.
5.2 Beskriv TALE-repeat genkendelse af nukleotider
Hvert TALE-repeat indeholder 34 aminosyrer og to alfa-helicer, men kun to aminosyre-rester er ansvarlige for unik genkendelse af et enkelt nukleotid i DNA-dobbelthelixen.
Tryk F4-F7 for at se hvordan TALE-repeats genkender specifikke nukleotider. Beskriv hvilke aminosyrer, der interagerer med hvilke baser og hvilken type interaktion der er tale om. Hvilken kant af baserne er involveret i interaktionen og hvilken af DNA-strengene genkendes?
5.3 Forslå protein-funktionaliteter for TALE
Man kan designe TALE-proteiner, så de binder til unikke DNA-sekvenser, ved at organisere rækkefølgen af TALE-repeats ihht. DNA-sekvensen.
Forslå hvilke protein-funktionaliteter man kan sætte i enden af et TALE-proteindomæne og beskriv hvilke biologiske effekter det kan have og/eller hvilke teknologiske muligheder det kan give.
6 Opgave 6. Trp trap træsko
I E. coli binder Trp-repressor en specifik DNA-sekvens under tilstedeværelse af aminosyren tryptofan (Trp) og hæmmer dermed udtryk af fem gener i trp-operon. Trp-repressor danner en homodimer, der binder til DNA-dobbelthelix via to alpha-helicer (kaldet “genkendelseshelicer”). Åben PyMOL-scriptet Trp.pml i PyMOL, der laver en strukturel alignment af Trp-repressor (bundet til Trp og DNA) med apo-formen af proteinet (ikke bundet til Trp eller DNA). F1 viser denne alignment.
6.1 Bestem Trp-repressors bindingsgroove
I hvilken groove af DNA binder Trp-repressor med de to genkendelseshelicer? Mål afstanden mellem de to genkendelseshelicer i 1TRO. Hvilken DNA-helix-parameter svarer denne afstand til og hvorfor observeres denne afstand typisk for transkriptionsfaktorer?
6.2 Undersøg Trp-bindings effekt på repressor
Hvilken del af proteinet påvirkes mest af binding til Tryptofan? Mål afstanden mellem de to genkendelseshelicer for apo-repressoren og beskriv hvilken effekt ændringen må forventes at have på binding af DNA.
6.3 Beskriv groove-mønstret for Trp-repressor
Brug groove-kode scriptet (DNA-groove.pml) til at vise DNA-dobbelthelixen som kuglemodel, hvor H-bindingsacceptorer er farvet røde, H-bindingsdonorer blå, metylgrupper grønne og ikke-polære hydrogenatomer gule. Skjul Trp repressor, så kun DNA dobbelthelix ses.
Hvad er karakteristisk ved mønsteret af H-bindingsdonorer og -acceptorer og hvad fortæller det om bindingen af Trp repressor?
6.4 Identificer Arg69’s base-interaktion
Tryk F2 for kun at se polære kontakter mellem genkendelseshelicer og DNA-dobbelthelix. Hvilken kant af basen interagerer Arginin-69 med? Hvilke typer af interaktioner ser man typisk bidrage til bindingsspecificitet mellem DNA og protein?
7 Opgave 7. Arc repressor
PyMOL-scripting opgave: I denne opgave skal I analysere DNA-protein binding i PyMOL. I vil lære hvordan man farver proteiner efter sekundær struktur og hvordan man finder polære bindinger mellem to selektioner.
Arc-repressor (PDB-ID: 1BDT) er en transskriptionsfaktor fra bakteriofag P22, der hæmmer dets eget gen arc. Arc-repressor binder kooperativt som to dimerer til et 21-basepar operator site. DNA operator-sekvensen er vist herunder, hvor TAGA-sekvensen er farvet grå. Det brudte palindroms pseudosymmetri-akse går igennem det centrale G-C basepar.
5'-ATAGTAGAGTGCTTCTATCAT-3'3'-TATCATCTCACGAAGATAGTA-5'
7.1 Lav script til Arc-repressor-analyse
Lav et script, der gør følgende:
Henter Arc-repressoren og viser DNA-protein komplekset med pseudosymmetri-akse langs PyMOLs y-akse. Gem scenen med navnet F1 (scene F1, store).
Lav en scene kaldet F2, der farver sekundær struktur (se nedenstående PyMOL info).
Lav en scene kaldet F3, der viser afstanden mellem de to bindingselementer. Hint: Brug distance-funktionen mellem to atom selektioner på aminosyrer i bindingselementerne og brug mode=0, se nedenstående PyMOL info.
Lav en scene kaldet F4, der viser DNAs interaktion med proteinet. Vis genkendelses-element (rest 8-14) og DNA (chain E+F) som sticks med element farver. Find nu hydrogenbindinger mellem genkendelses-element (rest 8-14) og DNA. Hint: Brug distance-funktionen mellem genkendelses-element og DNA med mode=2, se nedenstående PyMOL info.
Når man farver proteiner efter sekundær struktur er der ikke en samlet kommando, der gør det. Man er nødsaget til at farve hver type, altså alphahelicer, betastrands og loops, enkeltvis. Loops indeholder alle sekundære strukturer, der ikke er betastrands eller alphahelicer. I har tidligere lært at property selektoren for sekundær struktur er ss. PyMOLs navn for alphahelicer, betastrands og loops er hhv. h, s og l+"". Man ville altså farve loops hvide med kommandoen: color white, ss l+"".
Distance funktionen kan tage et ekstra argument kaldet mode, som har flere indstillinger, men de vigtigste er mode=0 og mode=2. Med mode kan man bestemme hvilken type interaktioner man vil medtage. mode=0 er default og er bare afstanden mellem alle punkter i de to selektioner. mode=2 viser udelukkende de polære bindinger mellem to selektioner. Læs mere her.
Brug nu dit script til at svare på de følgende spørgsmål.
7.2 Beskriv DNA-bøjning ved Arc-binding
Tryk F1. Bindingen af Arc-repressor påvirker DNA-dobbelthelixen og fører til en bøjning. Hvilken basestak-parameter (Liljas figur 5.16) beskriver bedst bøjning?
7.3 Beskriv sekundær struktur i DNA-binding
Tryk F2. Beskriv bindingen af Arc-proteinet til DNA. Hvilken type protein-sekundær struktur binder til hvilken groove på DNA dobbelthelixen? Beskriv hvordan du observerer hvilken groove der bindes.
7.4 Find DNA-helixparameter for afstanden
Tryk F3. Hvilken DNA-helix parameter svarer denne afstand til?
7.5 Identificer H-bindingspartnere i active site
Tryk F4. Hvilke aminosyrer hydrogenbinder til baserne? Hvilke andre typer af interaktioner bidrager til bindingsspecificitet?