TØ 16 – Kulhydrater og glykosylering af proteiner
1 Opgave 1. AB0-blodtypesystemet
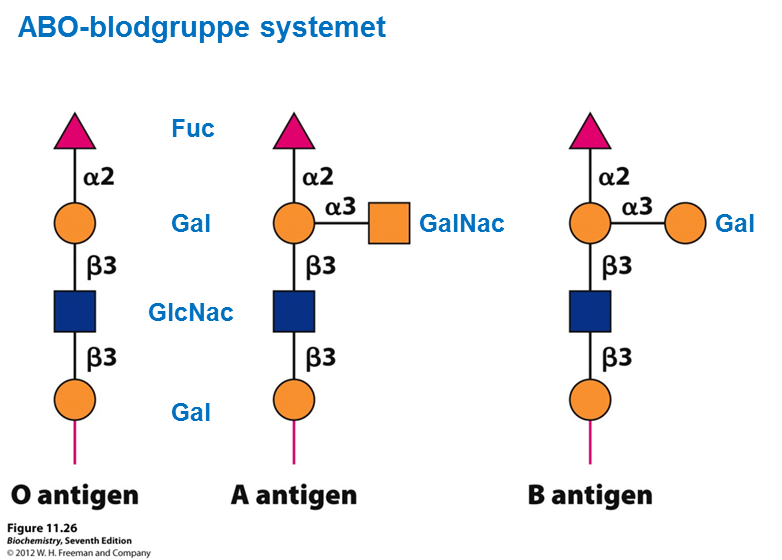
Hos mennesket udgør en lille gruppe af O-bundne oligosaccharider, som vist på figuren, blodtypesystemet AB0, hvor man som individ kan være af typen (og dermed udtrykke antigenerne) 0, A, B eller AB.
1.1 Beskriv biosyntese af O-bundne oligosaccharider
Beskriv hvordan modificerede proteiner af denne type syntetiseres. Sammenlign med biosyntesen af N-bundne oligosaccharider på glykoproteiner.
1.2 Beskriv genetik bag ABO-systemet
Beskriv det genetiske og biokemiske grundlag for at netop disse tre varianter dannes i det konkrete tilfælde med blodsystemet?
Erythropoeitin (EPO) er et glycoprotein der sitmulerer dannelse af røde blod legemer. EPO kan fremstilles recombinant i mammale celler hvorved man opnår et glykosyleret protein.
O- og N-glykosyleringer kan forudsiges ud fra aminosyresekvensen for et protein bl.a. via disse websites:
O-glykosyleringer: https://services.healthtech.dtu.dk/services/NetOGlyc-4.0/
N-glykosyleringer: https://services.healthtech.dtu.dk/services/NetNGlyc-1.0/
Gå til Uniprot, søg efter “human erythropoeitin” og kopier sekvensen (gå til “Sequence” , klik knappen FASTA og kopier sekvensen).
Undersøg sekvensen for mulige O- og N-glykosyleringer på ovenstående websites.
1.3 Forudsig N-glykosyleringer i EPO
Hvor mange N-glykosyleringer bliver der forudsagt?
1.4 Forudsig O-glykosyleringer i EPO
Hvor mage O-glykosyleringer bliver der forudsagt?
Sammenlign resultatet med Stryer Figur 11.17 (bemærk at der er forskel i sekvensnummereringen pga. af et signalpeptid) eller Uniprot under overskriften “PTM/Processing”.
1.5 Vurdér forudsigelsesnøjagtighed
Hvilken type af forudsigelse (O- eller N-glykosylering) er mest nøjagtig og hvorfor?
Sammensætningen af glykosyleringer er afhængig ikke kun af den organisme proteinet udtrykkes i men også af celletypen. Man vil derfor kunne undersøge en blodprøve for forekomst af udefrakommende (exogent) EPO.
1.6 Identificér exogent EPO
Foreslå to metoder til identificering af exogent EPO og forklar hvorfor de kan anvendes.
2 Opgave 2. Serine carboxypeptidase Y
En vakuolær protease fra gær, serine carboxypeptidase Y (CPY), er involveret i C-terminal forarbejdning af peptider og proteiner. Vakuoler er membranomsluttede vesikler i svampe og planter, der er vigtige for den intracellulære nedbrydning af affaldsprodukter, men CPYs præcise rolle i disse er uklar. CPY syntetiseres i en pre-pro form og bruges derfor som modelsystem for intracelullær proteinsortering i eukaryoter.
Aminosyresekvensen af pre-pro formen af CPY er vist nedenfor.
MKAFTSLLCG LGLSTTLAKA ISLQRPLGLD KDVLLQAAEK FGLDLDLDHL LKELDSNVLD
60
AWAQIEHLYP NQVMSLETST KPKFPEAIKT KKDWDFVVKN DAIENYQLRV NKIKDPKILG
120
IDPNVTQYTG YLDVEDEDKH FFFWTFESRN DPAKDPVILW LNGGPGCSSL TGLFFELGPS
180
SIGPDLKPIG NPYSWNSNAT VIFLDQPVNV GFSYSGSSGV SNTVAAGKDV YNFLELFFDQ
240
FPEYVNKGQD FHIAGESYAG HYIPVFASEI LSHKDRNFNL TSVLIGNGLT DPLTQYNYYE
300
PMACGEGGEP SVLPSEECSA MEDSLERCLG LIESCYDSQS VWSCVPATIY CNNAQLAPYQ
360
RTGRNVYDIR KDCEGGNLCY PTLQDIDDYL NQDYVKEAVG AEVDHYESCN FDINRNFLFA
420
GDWMKPYHTA VTDLLNQDLP ILVYAGDKDF ICNWLGNKAW TDVLPWKYDE EFASQKVRNW
480
TASITDEVAG EVKSYKHFTY LRVFNGGHMV PFDVPENALS MVNEWIHGGF SL
5322.1 Find N-glykosylerede positioner i CPY
CPY indeholder fire N-glykosylerede aminosyrerester. Angiv deres position og den lokale sekvens omkring dem.
2.2 Foreslå oligosaccharidstrukturer
Oligosacchariderne koblet til CPY er hovedsagelig på formen Glc3Man9GlcNAc2, Man8GlcNAc2 og Man5GlcNAc2. Foreslå strukturer for oligosacchariderne.
2.3 Analysér oligosaccharidstruktur eksperimentelt
Hvorledes kunne man eksperimentelt analysere strukturen af oligosacchariderne koblet til CPY?
Aminosyreresterne 1-20 udgør signalsekvensen i pre-pro CPY, hvorefter 21-111 er pro-peptidet og 112-532 udgør selve enzymet. I sekvensen finder man yderligere et konsensussignal for vakuolær sortering, QRPL.
2.4 Beskriv modning af CPY
Beskriv ud fra de givne oplysninger, hvordan modningen af CPY i cellen kunne foregå.
3 Opgave 3. Mannosidase I
Mannosidase I er et enzym der fjerner mannose enheder fra høj-mannose glycosyleringen der bliver tilføjet i ER. Den er således en forudsætning for at yderligere modificering af glycosyleringer senere kan foregå i Golgi. Mannosidase I er specific for α1-2 glycosid bindinger.
3.1 Beskriv stub efter mannosidase I
Hvorledes vil den fælles N-glycosylerings stub se ud efter behandling med mannosidase I?
3.2 Find fucosyleringens placering
PNGase-F (peptide N-Glycosidase F) anvendes i laboratoriet ofte til at fjerne N-glycosyleringer fra proteiner idet den kløver N-glycosid bindingen mellem asparagine og N-acetylglucosamine. Denne kløvning sker imidlertid ikke hvis glykosyleringen indeholder en fucosylering.
Hvor er fucosyleringen sædvanligvis placeret i en N-glycosylering ?
3.3 Forklar PNGase F-specificitet
Hvorfor kan PNGase F ikke kløve en fucosyleret glycosylering ?
3.4 Vurdér effekt af kifunensin
Kifunensin er en inhibitor af mannosidase I. I forbindelse med udtryk af proteiner i mammale cellekulturer tilsættes kifunensin ofte til mediet.
Vil det have en effekt på effektiviteten af efterfølgende PNGase-F behandling ?
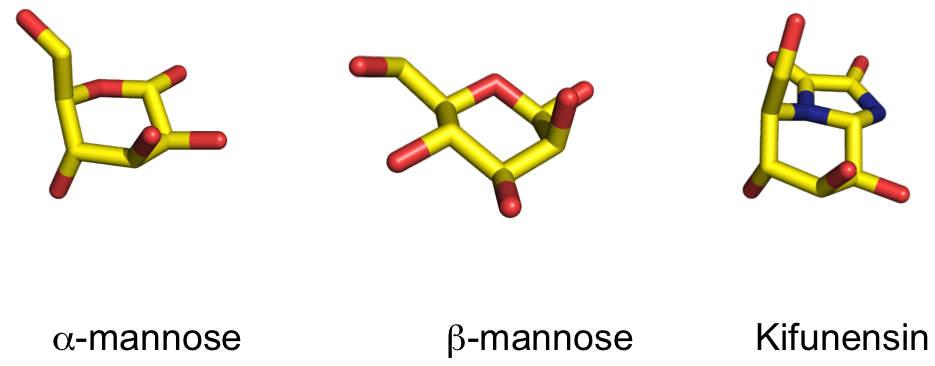
Nedenfor er vist strukturen af alpha-D-mannopyranose, beta-D-mannopyranose og kifunensin.
3.5 Klassificér kifunensin som inhibitor
Vil du forvente at kifunensin er en kompetitiv, non-kompetitiv eller un-kompetitiv inhibitor ?
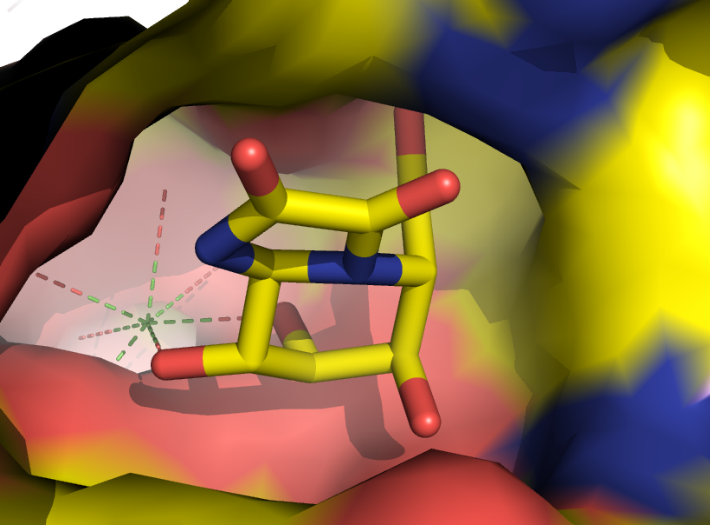
I billedet nedenfor er vist kifunensin bundet i en lomme i mannosidase I. Kifunensin er vist som sticks og enzymet som en overflade. Det grønne kryds er en Ca2+ ion og de stiplede linier angiver interaktioner med oxygen atomer.
3.6 Forklar α-glycosidbindingsspecificitet
Forklar hvorfor Mannosidase I er specifik for α-glycosid bindinger.
4 Opgave 4. Glykosyleringer i sortilin
I forbindelse med bestemmelse af krystalstrukturen af glycoproteiner behandler man ofte proteinet med enzymet PNGase F (peptide N-Glycosidase F) inden krystallisation.
4.1 Forklar rationalet for PNGase F-behandling
Hvad er rationalet bag denne behandling?
4.2 Vis sortilins glykosylerede asparaginer
Sortilin er en endocytose-receptor som er i stand til at binde et antal forskellige ekstracellulære proteiner og peptider og transportere dem til lysosomer. Ved bestemmelse af krystalstrukturen (PDB-ID: 4PO7) blev sortilin ikke behandlet med PNGaseF.
Lav en scene, kaldet F1, som viser cartoon repræsentation og en scene, kaldet F2, der viser sortilins overflade. Hvilke asparaginer kan ses at være glycosyleret i Sortilin?
4.3 Find N-glykosyleringssites i Uniprot
Bemærk at surface-repræsentation kun ændrer proteinets repræsentation, men at solvent og glycosyleringer fortsat vises som sticks.
Find aminosyresekvensen for humant sortilin på Uniprot. Bemærk: der er forskel på nummereringen i UNIPROT og i PDB-ID: 4PO7.
Hvor mange N-glykosyleringssites siger Uniprot der er i humant sortilin?
4.4 Forklar manglende glykosylering
Hvorfor er det ikke alle N-glykosyleringssites der ses at være glycosyleret i krystalstrukturen?
4.5 Sammenlign behandlet og ubehandlet sortilin
Ved bestemmelse af en anden krystalstruktur af sortilin (PDB-ID: 3F6K) blev sortilin behandlet med PNGaseF inden krystallisation.
Overlejr den behandlede sortilin med den ubehandlede sortilin og kald scenen F3. Lav så scener, kaldet F4, F5 og F6, som viser de 3 glycosylerede sites.
Hvorfor er det kun dele af glycosyleringerne, der fjernes?
4.6 Beskriv glycosylering på Asn549
Beskriv opbygningen af glycosyleringen på Asn549 på den ubehandlede sortilin og lav en scene kaldet, F7, som viser denne. Hint: definer Asn og glycolysering som et objekt. Dette inkluderer karakterisering af glycosidbindingerne.
4.7 Vis hydrogen-bindinger til glycosylering
Vis nu sortilin som regnbuefarvet ‘cartoon’ og find polære kontakter mellem glykosyleringen på Asn549 og protein delen af sortilin.
Lav en scene, kaldet F8, der viser dette. Hvilke sidekæder danner hydrogen-bindinger med glykosyleringen?
4.8 Forklar manglende udtryk af mutant
I et forsøg på at fjerne alle glykosyleringer blev alle asparaginer, der var forudsagt til at være glycosyleret i sortilin, muteret til alanin. Imidlertid viste det sig efterfølgende at det muterede sortilin ikke blev udtrykt.
Giv en mulig forklaring på denne observation.
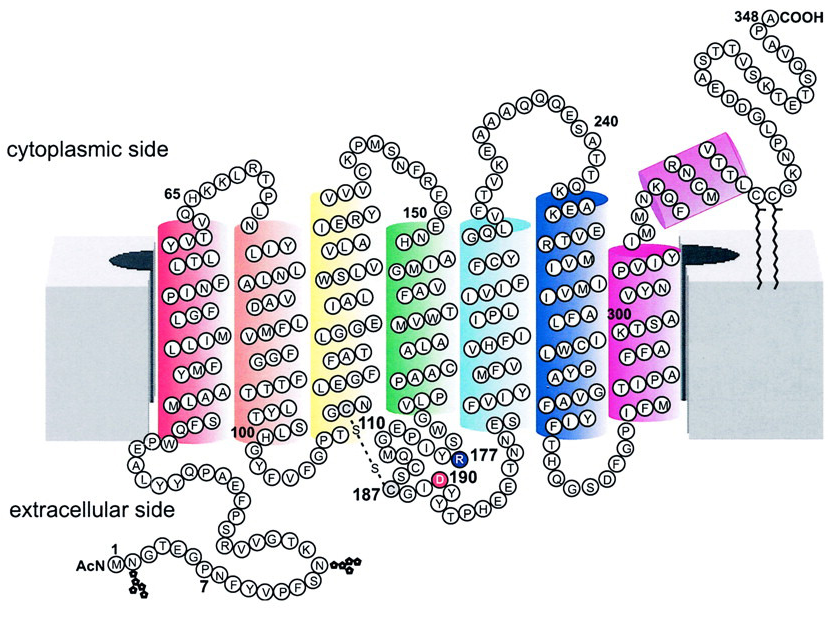
5 Opgave 5. (Rhod-)opsin (PyMOL)
Proteinet rhodopsin er ansvarlig for omsætning af lys til et sansesignal i øjet. Strukturbestemmelse af rhodopsin har været ekstremt udfordrende, da proteinet ikke blot er et membranprotein, men heller ikke tåler lys. Derfor skal oprensningen ske i mørke.
5.1 Hent og visualisér rhodopsin
Lav et script, der henter krystalstrukturen af bovine rhodopsin bestemt til en opløsning af 2,2 Å (PBD-ID: 1U19) og opret et objekt, der kun indeholder kæderne A, C og D. Vis strukturen som cartoon i regnbuefarve (N=blå til C=rød), vis ioner som kugler og andre ligander med sticks. Gem dette som en scene kaldet F1.
Beskriv den overordnede foldningsklasse og struktur af rhodopsin.
Man kan med fordel bruge RCSB til at finde positioner for ligander / kigge på sekvensen i PyMol for residue numre/navne.
5.2 Beskriv N-glykosyleringers kobling
Kæderne C og D indeholder ikke protein, men er kovalent koblede til det. Hvordan er kæderne C og D koblet til rhodopsin og hvad indeholder de? Beskriv den modulære opbygning af kæderne.
5.3 Identificér PLM-ligander
Strukturen indeholder to molekyler med betegnelsen PLM. Hvilket stof er der tale om og hvorfor tror du det binder til rhodopsin?
5.4 Vis og beskriv retinal-binding
Identificér den prostetiske 11-cis retinal-gruppe og lav en scene kaldet F2, som tydeligt viser denne. Beskriv interaktionen mellem 11-cis retinal og rhodopsin. Hvordan fastholdes den protestiske gruppe? Hvor er den optisk aktive del af 11-cis retinal?
5.5 Sammenlign rhodopsin og opsin
Hent strukturen af opsin (PDB-ID: 3CAP) og på samme måde som før; dan et objekt med kæderne A, C og D. Foretag dernæst en overlejring af opsin på rhodopsin. Gem dette som scene F3. Hvad er forskellen på opbygningen af opsin og rhodopsin? Giver denne forskel anledning til strukturelle ændringer? Hvilke?