TØ 13 – Enzymregulering
1 Opgave 1. LDH-isozymer
Søg efter “LDH human” på www.uniprot.org.
Undersøg de relevante resultater. Se under overskriften “Sequences” og følg evt. link til Ensembl eller GeneID under overskriften “Genome Annotation Databases”
1.1 Find antal LDH-isoformer i UniProt
Hvor mange isoformer findes for LDH i menneske?
1.2 Find betegnelser for LDH-varianter
I Stryer betegnes to former af LDH som henholdsvis H og M form.
Hvordan betegnes disse to varianter i Uniprot?
1.3 Find kromosomer for LDH-generne
På hvilke kromosomer finder man generne for de to former?
1.4 Tæl splejsningsvarianter af LDH-M
Hvor mange splejsningsvarianter kendes for LDH-M?
2 Opgave 2. Aspartat
Aspartat er substrat for enzymet, aspartat transcarbamoylase (ATCase), og enzymet kan inhiberes ved tilsætning af phosphonacetyl-L-aspartat (PALA; Ki = 10 nM).
2.1 Bestem PALA’s inhibitionstype og styrke
Hvilken type inhibering udøver PALA? Er PALA en svag, medium eller stærk inhibitor?
2.2 Beskriv aktiveringseffekt ved PALA
Stimulering af ATCase-aktiviteten kan observeres under visse eksperimentelle betingelser, som vist nedenfor.
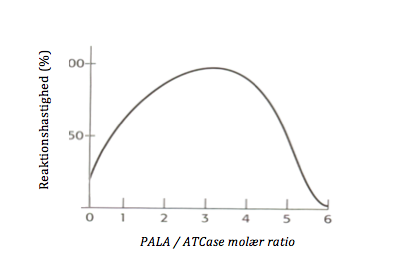
Beskriv kurven og forklar hvad der foregår.
2.3 Identificer pathway påvirket af mutationen
En E. coli-mutant indeholdende en enzymdefekt relevant for biosyntesen af threonin, isoleucin og methionin kan kun gro hvis vækstmediet suppleres med de tre aminosyrer. Selv under disse betingelse er væksten reduceret, hvilket formodentlig skyldes akkumulering af et mellemprodukt. Hvis man derimod tilsætter uracil, ses en normal vækstrate. (Hint: Læs om homoserine dehydrogenase på wikipedia)
Hvilken anden pathway kunne være influeret af mutationen og hvorfor?
Kig på reaktionspathwayen for threonin, isoleucin og methionin.
3 Opgave 3. ATCase
ATCase er et eksempel på et vigtigt allosterisk reguleret enzym. Åben filen ATCase.pml, der findes i mappen for denne uge i Brightspace. Knapperne T_trimer1, T_trimer2, T_dimer1, T_dimer2, and T_dimer3 kan bruges til at tænde og slukke for enkelte subunits i T-tilstanden (F1). Tryk på F2 for at skifte til R-tilstanden. F3 og F4 er side-views af hver tilstand. F5 og F6 viser backbone i T- og R-tilstanden. F7 er et overlay af T- og R-trimer backbone.
3.1 Beskriv ATCases T-til-R-overgang
Beskriv de strukturelle ændringer, der finder sted i ATCase når enzymet skifter mellem T- og R-tilstanden.
3.2 Identificer hvilke subunits binder ligander
T-tilstanden er bundet til ATP i denne struktur, mens R-tilstanden binder N-(phosphonacetyl)-L-aspartate (PALA). Hvilken type subunit binder ATP hhv. PALA til?
3.3 Forklar PALA’s analytiske anvendelighed
Hvorfor har PALA været specielt nyttig i forhold til at forstå ATCases egenskaber?
3.4 Forklar PALA som aktivator og inhibitor
Forklar hvordan PALA kan fungere både som en aktivator og en inbitor af ATCase.
4 Opgave 4. Thrombin og Antithrombin (PyMOL)
PyMOL-opgave: I denne opgave vil i blive introduceret for analyse af elektrostatiske overflader. I vil også få beskrevet hvordan man laver en log-file og bruger den til at bestemme kommandoer.
Selv om thrombin har mange egenskaber til fælles med trypsin, så er omdannelsen af prothrombin til thrombin ikke autokatalytisk som set for aktiveringen af trypsin. Både thrombin og trypsin er serinproteaser, der er i stand til at kløve peptidbindingen på carboxylsiden af arginin. Thrombin er dog specifik for Arg-Gly bindinger.
4.1 Forklar ikke-autokatalytisk aktivering
Hvorfor er aktiveringen af prothrombin til thrombin ikke autokatalytisk.
4.2 Sammenlign thrombins og trypsins substratgenkendelse
Beskriv ligheder og forskelle mellem den måde de to enzymer genkender deres substrat på.
4.3 Identificer heparins kemiske gruppe
Heparin er en højt sulfateret glycosaminoglycan polymer, der bnder til mange af proteinerne i koagulationskaskaden og påvirker aktiviteten af serpiner som antithrombin. Det bruges indenfor lægevidenskaben til at behandle bl.a. thrombose (dannelse af blodklumper i blodet) og som et additiv til donorblod, for at modvirke koagulation under oplagring. Den kemiske struktur af en heparinenhed er vist nedenfor.
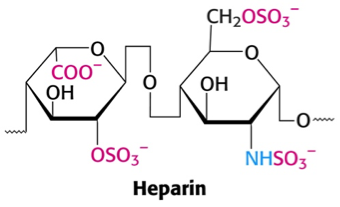
Hvilken gruppe af stoffer tilhører heparin og hvilke funktionelle grupper indeholder det?
4.4 Forudsig heparins bindingspartnere
Hvilken type af sidekæder vil du forvente at heparin binder til?
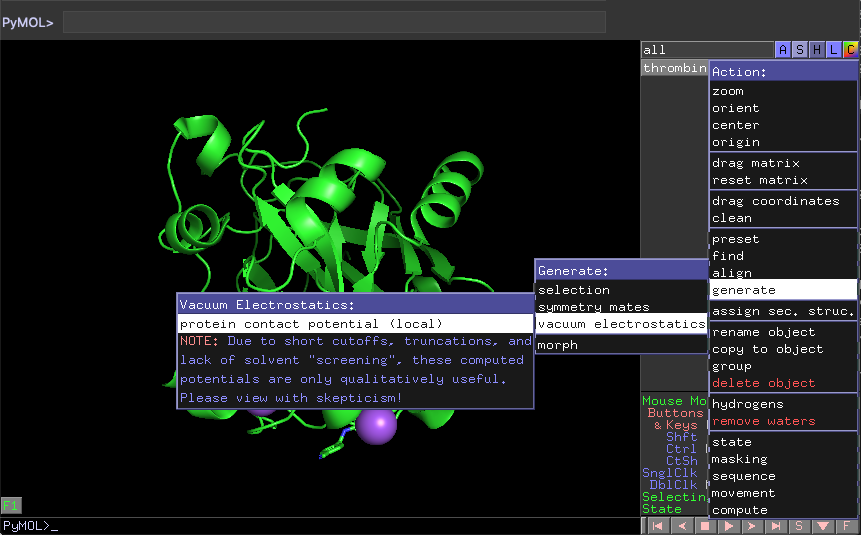
Vi skal nu visualisere den elektrostatiske overflade. Når man bruge PyMOL-interface tastes; A>generate>vacuum electrostatics>protein contact potential (local). Se figuren forneden.
Men vi vil ikke bare gøre det i vores PyMOL session. Vi vil have det ind i vores script.
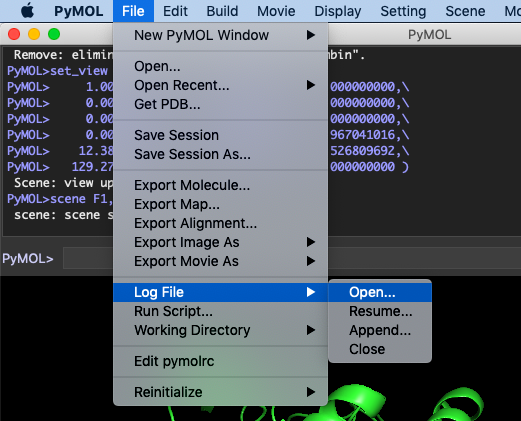
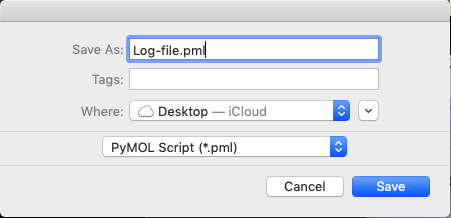
Når man skal bestemme kommandoen for en mere kompliceret funktion vil det ofte være smart åbne en logfil. Det gør man som illustreret for neden ved at gå ind på undermenuen File, derefter på Log File og til sidst Open\.... Så gemmer du det under det ønskede navn, f.eks. Log-file.pml.
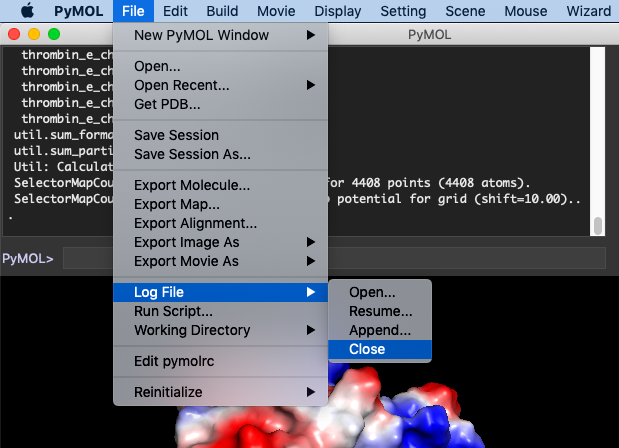
Herefter bruger du A>generate>vacuum electrostatics>protein contact potential (local) igen. Herefter går du ind og lukker logfilen som du ser i figuren forneden.
Herefter vil du kunne gå ind på log-filen og se kommandoen for den aktion du lige har udført. Denne kan bruges i dit script.
Positionen af den elektrostatiske overflade beregnes ligesom den vand-tilgængelige overflade og så farves den efter elektrostatisk potentiale. Potentialet beregnes som den tiltrækning (blå) eller frastødning (rød) en negativ punktladning vil opleve hvis den blev placeret på overfladen af proteinet. Beregningen foretages for neutralt pH.
4.5 Visualiser thrombins elektrostatiske overflade
Lav en scene, kaldet F1, som henter thrombin (PDB-ID: 3UTU). Lav så en scene, kaldet F2, som viser den elektrostatiske overflade af thrombin. Foreslå et bindingsite for heparin på overfladen af thrombin.
Strukturen af thrombin i kompleks med inhibitor og et heparin fragment findes i PDB-ID: 1XMN.
4.6 Sammenlign heparins bindingssite i PyMOL
Lav en scene, kaldet F3, som viser heparins binding til thrombin (PDB-ID: 3UTU).
Brug align og util.protein_vacuum_esp. Stemmer heparins placering overens med det forventede bindingsite?
5 Opgave 5. Antithrombin
En anden faktor, der deltager i koagulationskaskaden er factor XIa. Som andre proteaser i blodet reguleres factor XIa af en inhibitor, antithrombin III, der er medlem af familien af serineproteaseinhibitorer (serpiner).
5.1 Forklar behovet for antithrombin
Hvorfor har kroppen brug for en inhibitor som antithrombin?
5.2 Analyser heparins effekt på serpinaktivitet
Figuren nedenfor viser resultaterne fra et eksperiment, hvor effekten af antithrombin III på factor XIa’s proteolytiske funktion blev målt, med og uden heparin tilstede.
Hvordan påvirker heparin serpinens aktivitet?
5.3 Visualiser antithrombin-thrombin-komplekset
Mange af faktorerne i koagulationskaskaden har samme foldning. Det gælder for thrombin og factor XIa. Strukturen af et kompleks mellem antithrombin, Thrombin og en heparin-analog findes i PDB-ID: 1TB6.
Fortsæt scriptet fra opgave 4. Lav en scene, kaldet F4, som nedhenter komplekset og viser antithrombin og thrombin i forskellige farver. Lav så en scene, kaldet F5, som viser heparins binding til antithrombin/thrombin-kompleksets overflade. Forklarer denne struktur effekten af heparin?
5.4 Sammenlign heparinbinding på factor XIa
Strukturen af factor XIa findes i PDB-ID: 3SOR. Lav en overlejring af 3SOR på thrombin i 1TB6.
Lav en scene, kaldet F6, der viser XIa’s interaktion med heparin. Vil man forvente at heparin binder på samme måde til Factor XIa som til thrombin?
6 Opgave 6. Kløvning af thrombin med factor Xa
Nedenfor ses aminosyresekvensen for thrombin:
10 20 30 40 50 60
MARVRGPRLP GCLALAALFS LVHSQHVFLA HQQASSLLQR ARRANKGFLE EVRKGNLERE
70 80 90 100 110 120
CLEEPCSREE AFEALESLSA TDAFWAKYTA CESARNPREK LNECLEGNCA EGVGMNYRGN
130 140 150 160 170 180
VSVTRSGIEC QLWRSRYPHK PEINSTTHPG ADLRENFCRN PDGSITGPWC YTTSPTLRRE
190 200 210 220 230 240
ECSVPVCGQD RVTVEVIPRS GGSTTSQSPL LETCVPDRGR EYRGRLAVTT SGSRCLAWSS
250 260 270 280 290 300
EQAKALSKDQ DFNPAVPLAE NFCRNPDGDE EGAWCYVADQ PGDFEYCDLN YCEEPVDGDL
310 320 330 340 350 360
GDRLGEDPDP DAAIEGRTSE DHFQPFFNEK TFGAGEADCG LRPLFEKKQV QDQTEKELFE
370 380 390 400 410 420
SYIEGRIVEG QDAEVGLSPW QVMLFRKSPQ ELLCGASLIS DRWVLTAAHC LLYPPWDKNF
430 440 450 460 470 480
TVDDLLVRIG KHSRTRYERK VEKISMLDKI YIHPRYNWKE NLDRDIALLK LKRPIELSDY
490 500 510 520 530 540
IHPVCLPDKQ TAAKLLHAGF KGRVTGWGNR RETWTTSVAE VQPSVLQVVN LPLVERPVCK
550 560 570 580 590 600
ASTRIRITDN MFCAGYKPGE GKRGDACEGD SGGPFVMKSP YNNRWYQMGI VSWGEGCDRD
610 620
GKYGFYTHVF RLKKWIQKVI DRLGS
Factor Xa aktiverer prothombin til thrombin ved kløvning af peptidbindingerne efter Arg317 og Arg366.
6.1 Bestem factor Xa’s substratspecificitet
Hvad er factor Xa’s substratspecificitet? Resterne 409, 465 og 571 er vist med fed skrift i sekvensen ovenfor. Hvilke aminosyrer er der tale om og hvilken rolle spiller de i henholdsvis prothrombin og thrombin?
6.2 Skitsér SDS-PAGE af prothrombin-aktivering
Skitsér hvorledes prothrombin ville løbe i en SDS polyacrylamide gel under reducerende betingelser, før og efter aktivering med factor Xa. Forestil dig, at gelen farves med Coomassie Blue og markér hvert bånd med den forventede molekylemasse.
6.3 Forklar factor XIIIa’s stabilisering af blodklump
Hvordan bidrager factor XIIIa til stabilisering af en blodklump?