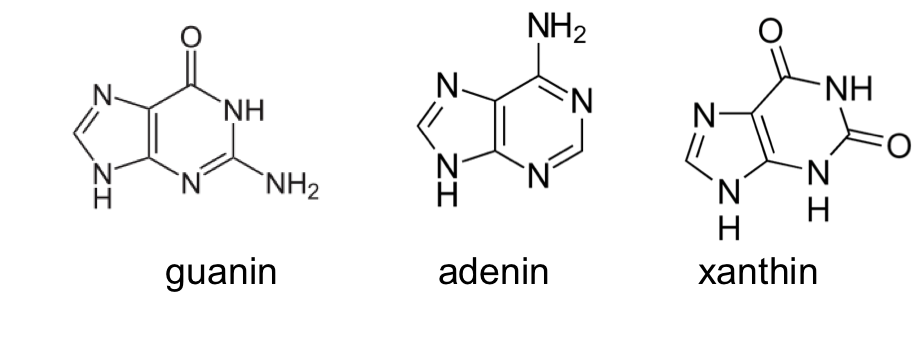TØ 4 – Proteinstruktur 1
1 Opgave 1. UniProt-databasen - Chymotrypsin
UniProt (www.uniprot.org) er en database over kendte proteinsekvenser. Hver enkelt sekvens i databasen er i vidt omfang annoteret og krydsrefereret til andre databaser.
Gå til UniProt og søg efter “bovine chymotrypsinogen A”.
Klik på det øverste hit på listen (P00766). Til venstre på siden ses nu en kolonne, der kontrollerer visningen på højre del af siden. Som default er de alle vinget af. Klik på “Sequence” eller rul ned på siden til du kommer til overskriften “Sequence”.
Til højre på siden er der information om sekvenslængde og molekylevægt. Desuden er der mulighed for yderligere beregninger ved at vælge fra dropdown-menuen til venstre for GO knappen.
1.1 Tæl aminosyrerester i chymotrypsinogen
Hvor mange aminosyrerester er der i sekvensen?
1.2 Find molekylvægt af chymotrypsinogen
Hvad er molekylvægten (\(M_w\)) for den viste sekvens?
Den viste sekvens er for chymotrypsinogen, som efter aktivering ved proteolytisk kløvning danner det aktive α-chymotrypsin (se Stryer, Fig. 10.18, s. 324).
Her er det nødvendigt at oprette et “fragment”, der dækker hele chymotrypsinogens sekvens nederst på ProtParam-siden.
1.3 Tæl helixer i α-chymotrypsin
Hvor mange helixer er der i α-Chymotrypsin?
Klik på “Structure” til venstre på UniProt-siden
1.4 Find molekylvægt af α-chymotrypsin
Hvad er \(M_w\) for α-chymotrypsin?
Brug “ProtParam” fra dropdown-menuen i “Sequence”-afsnittet af UniProt til at beregne molekylvægten for hver af de tre kæder i aktivt α-chymotrypsin.
ProtParam beregner også aminosyresammensætning for sekvensen.
1.5 Find de tre største aminosyreafvigelser
Hvad er de tre største afvigelser mellem chymotrypsinogens aminosyresammensætning og sammensætningen for gennemsnittet af proteiner (https://web.expasy.org/docs/relnotes/relstat.html nederst på siden)? Kan nogle af disse forskelle forklares udfra dit kendskab til enzymet?
Her er det nødvendigt at oprette et “fragment”, der dækker hele chymotrypsinogens sekvens nederst på ProtParam-siden.
1.6 Tæl helixer i α-chymotrypsin
Hvor mange helixer er der i α-Chymotrypsin?
Klik på “Structure” til venstre på UniProt-siden
2 Opgave 2. Ramachandran-plottet
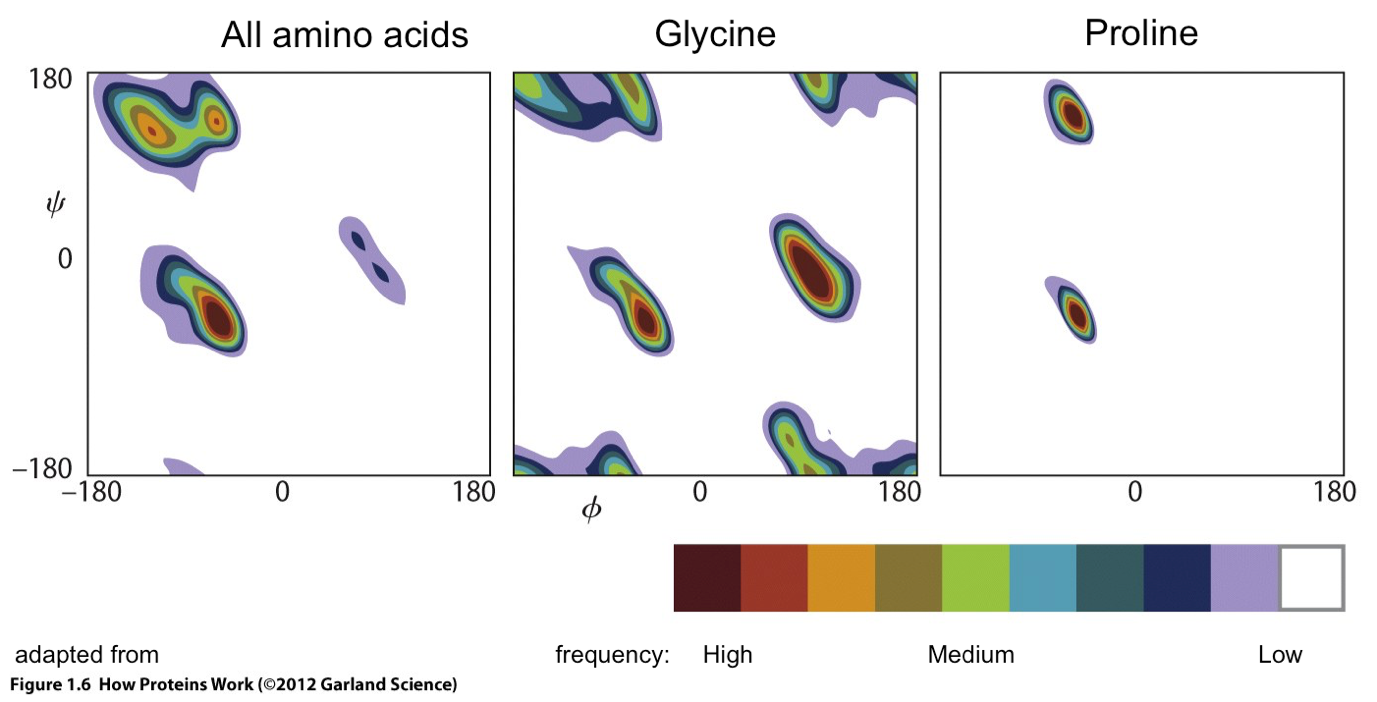
På figuren nedenfor er vist fordelingen af phi \(\phi\) og psi \(\psi\) vinkler for aminosyrerester i kendte protein strukturer (Hovmöller et al., Acta Cryst D, 58, p.768-776, 2002). Til venstre er vist den generelle fordeling for alle aminosyrer, dernæst for glycin rester og længst til højre for prolin rester.
2.1 Forklar Pro og Gly i Ramachandran-plottet
Hvilke strukturelle egenskaber for Pro og Gly forklarer deres placeringer i Ramachandran-plottet?
2.2 Identificer tre områder med høj forekomst
På figuren for alle aminosyrer er der tre områder med høj forekomst af aminosyrerester. Hvor finder man typisk disse områder i proteiners sekundærstruktur
3 Opgave 3. C-alpha diagram
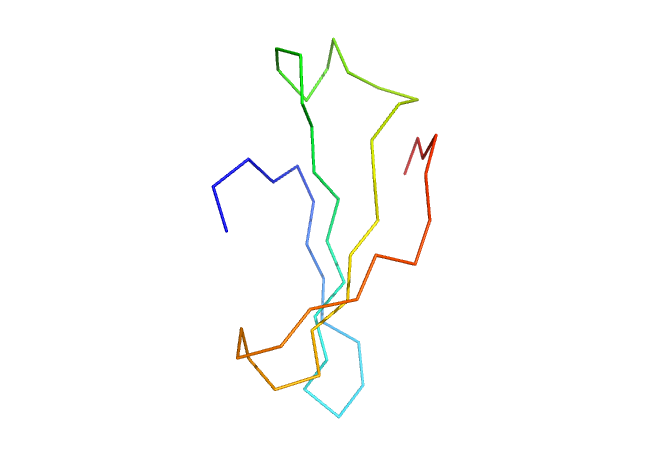
Nedenfor er vist et Cα-diagram for en struktur farvekodet efter de sædvanlige konventioner. Strukturen indeholder en β-plade bestående af fire β-kæder og proteinet har følgende sekvens:
HKAVCLAKWGSDNTIFFTTYANGSCKADLGALLELWRTSDLGKSFKTIGVKIYS3.1 Afmærk N- og C-terminus i diagrammet
Afmærk positionen af N- og C-terminus og forklar hvordan dette kan ses.
3.2 Afmærk de to valin-rester
Afmærk positionen af de to valin-rester i sekvensen og forklar hvordan dette kan ses.
3.3 Angiv β-kædernes position og retning
Angiv den omtrentlige position af β-kæderne og deres retning. Forklar dit svar.
3.4 Bestem β-kædernes parallelitet
Er β-kæderne parallelle eller anti-parallelle?
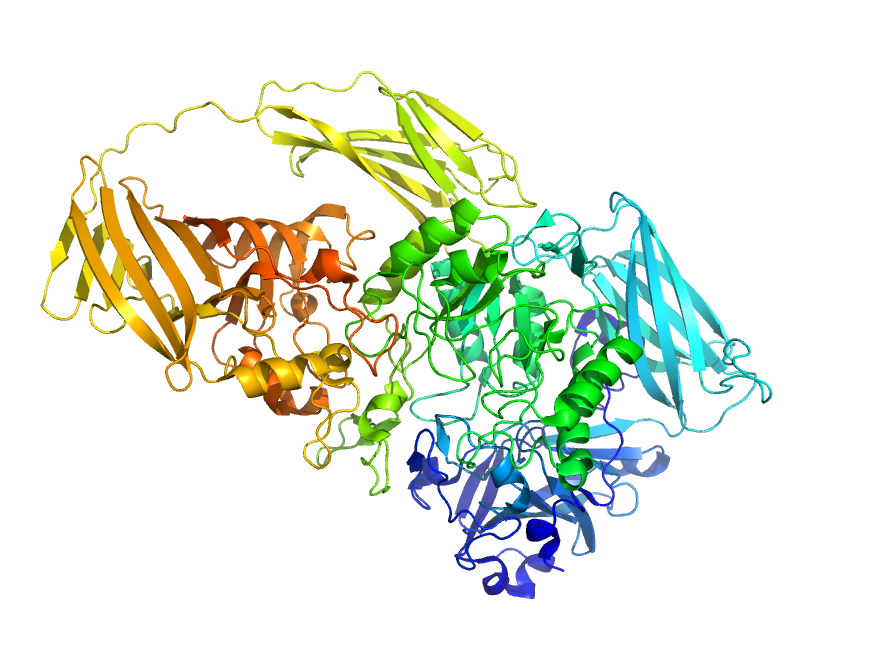
4 Opgave 4. Cartoons
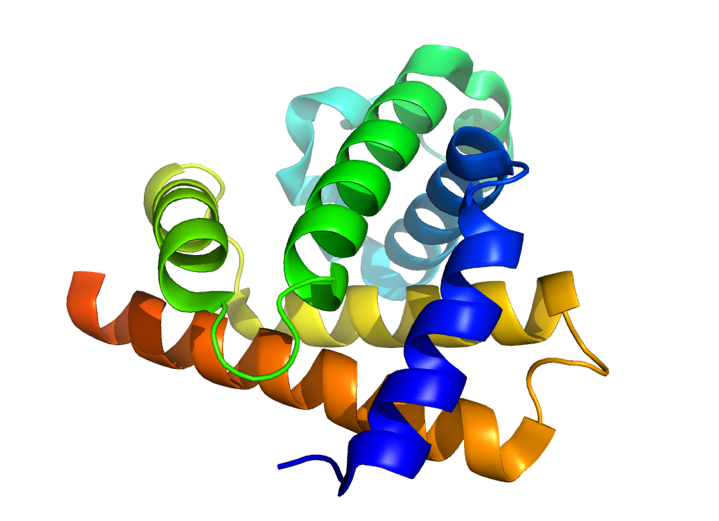
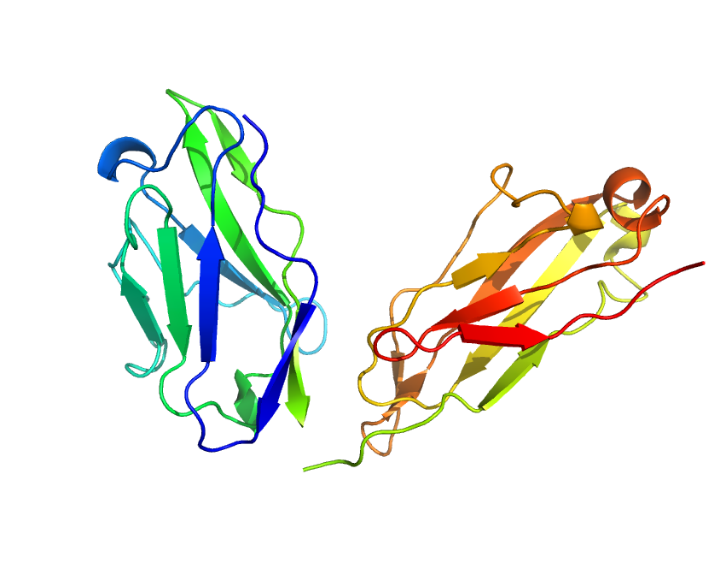
Strukturerne af proteinet myoglobin, et immunoglobulin Fab-fragment samt β-galactosidase er vist nedenfor som cartoons.
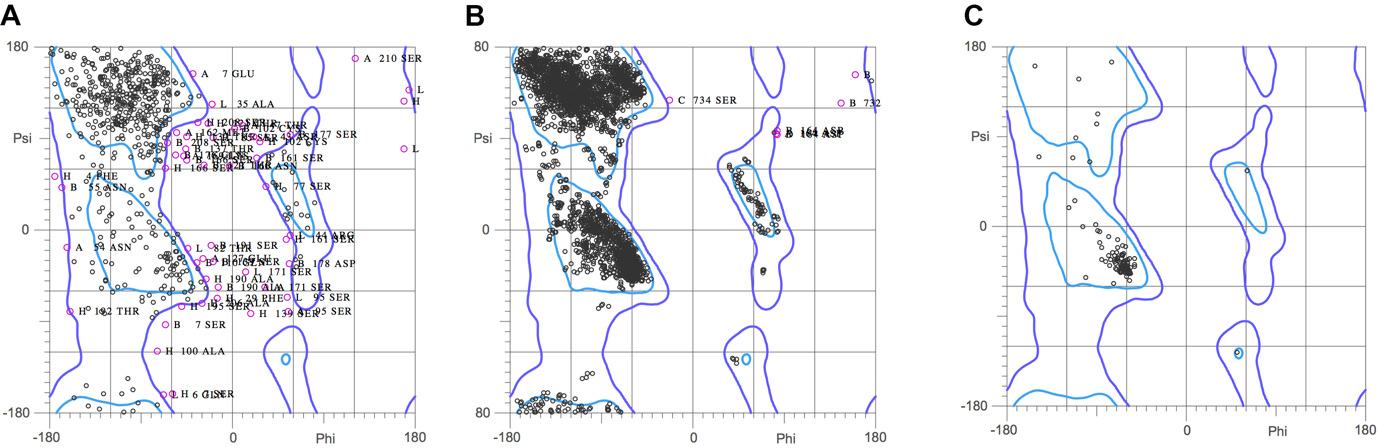
Ramachandran-plot for de tre strukturer er mærket A, B, og C og vist herunder.
Hvilken struktur hører til hvilket plot?
Forklar dit svar.
5 Opgave 5. Afstand mellem C-alpha atomer
5.1 Tegn trans-peptidbinding med mål
Tegn en trans-peptidbinding med korrekte bindingslængder (se Berg, 10. udgave, s. 44) i en fast målestok (f.eks. 1 Å : 2 cm). Brug 120° som bindingsvinkel mellem alle tre bindinger til C (carbonyl-kulstof) og N (amid-nitrogen), da begge er sp2-hybridiserede (dvs. det er plane grupper).
5.2 Tegn cis-peptidbinding med mål
Gentag ovenstående øvelse for en cis-peptidbinding.
5.3 Mål Cα-afstand i trans-peptid
Hvad er afstanden mellem de to Cα-atomer i et trans-peptid?
5.4 Mål Cα-afstand i cis-peptid
Hvad er afstanden mellem de to Cα-atomer i et cis-peptid?
6 Opgave 6. Binding af guanine
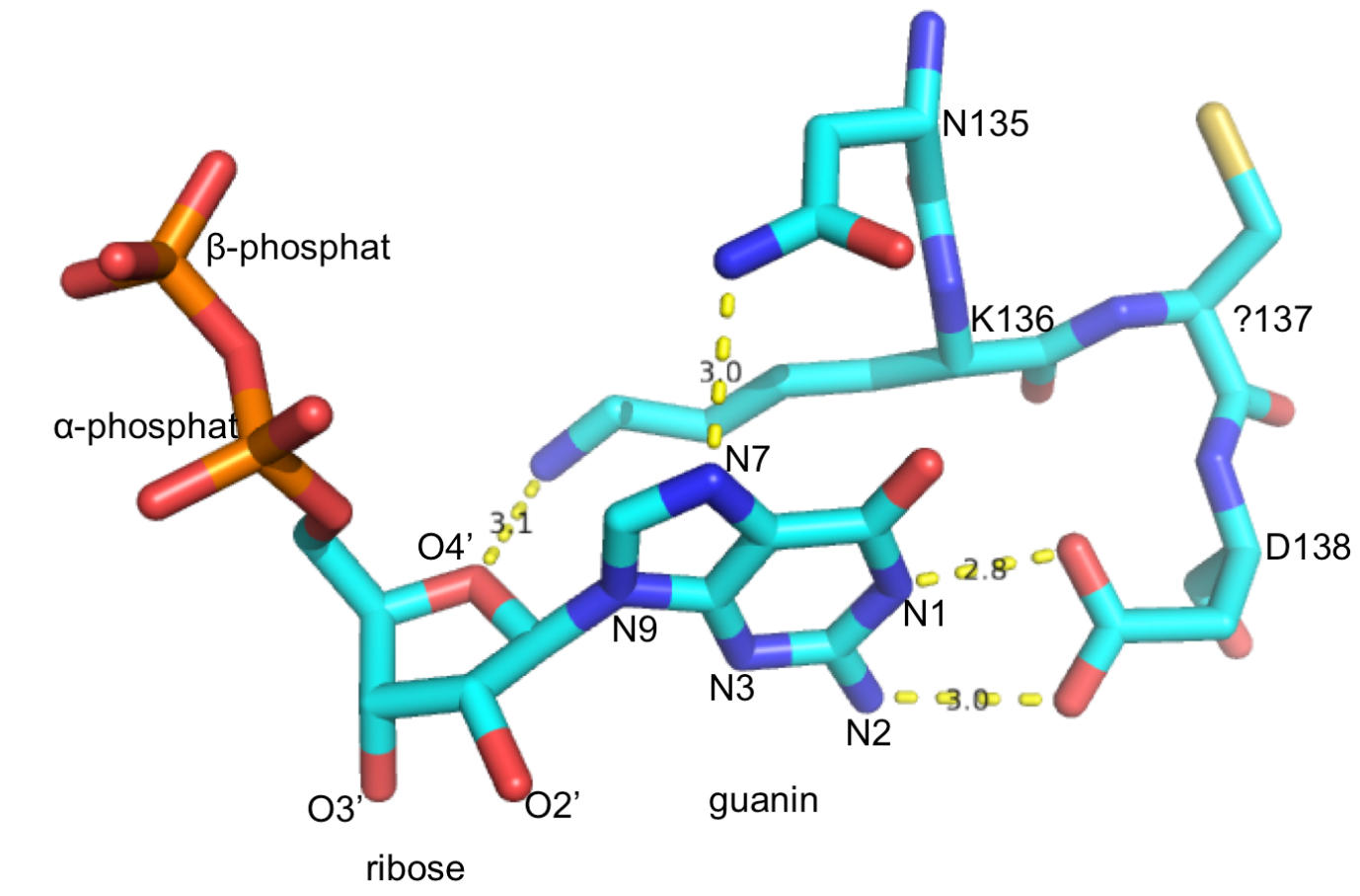
Alle GDP-bindende proteiner indeholder et bestemt sekvensmotiv, Asn-Lys-X-Asp (NKXD), og i strukturer af GDP-bindende proteiner finder man at sidekæderne i motivet er ansvarlige for genkendelse af selve guaninbasen. I figuren nedenfor ses et udsnit af det GDP-bindende protein EF-Tu (Elongeringsfaktor Tu), som viser bindingen af guanin- og ribose-delen af GDP (carbon - turkis, nitrogen – blå, oxygen - rød, svovl – gul, phosphor - orange, stiplede gule linjer viser hydrogenbindinger med angivelse af donor-acceptor afstand).
6.1 Find X i NKXD-motivet
Hvilken aminosyrerest svarer til X i NKXD motivet i dette tilfælde?
6.2 Analysér hydrogenbindinger til guanin
Analysér hydrogenbindingerne mellem sidekæderne og guanin og udfyld en tabel som den vist nedenfor
| Aminosyrerest (e.g. N135) |
Atom (e.g. Nζ) |
GDP atom (e.g. O3’) |
H-donor (p for protein, G for guanin) |
|---|---|---|---|
EF-Tu er specifik for binding af GDP og binder således hverken nukleotiderne ADP (adenosine diphosphate) eller XDP (xantosine diphosphate). De tilsvarende tre baser er vist nedenfor.
6.3 Forklar EF-Tu’s nukleotidspecificitet
Forklar hvordan denne specificitet opnås.
En mutation af aspartat til asparagin i sekvensmotivet for guaninbinding medfører at det muterede protein binder XDP og ikke GDP.
6.4 Forklar mutantens ændrede specificitet
Kom med en biokemisk forklaring på mutantens ændrede specificitet.
7 Opgave 7. Nukleotid binding
🧬 Download Elongerings_Faktor_Tu.pml
PyMOL-scripting opgave: I denne opgave skal i bruge de kommandoer I allerede kender, men også lære kommandoen “distance”.
Brug PyMOL scriptet Elongerings_Faktor_Tu.pml til at lave en figur af GDP-binding til Elongerings Faktor Tu fra E.coli (PDB-ID: 1EFC).
Strukturen af EF-Tu med GDPNP er også blevet bestemt (PDB-ID: 1EFT). I 1EFT er det EF-Tu fra den thermophile bakterie T.aquaticus. Da det er EF-Tu fra forskellige organismer er der forskel i sekvensnumrene for de sidekæder der indgår i binding af nukleotidet.
I scriptet indgår en linie:
select sidechains, byres eftu within 4.0 of nucleotide7.1 Forklar PyMOL select-kommandoen
Forklar betydningen af de enkelte elementer i den pågældende linie. Hint: se https://pymolwiki.org/index.php/Select og https://pymolwiki.org/index.php/Selection_Algebra
I er tidligere blevet introduceret for Wizard-measurement funktionen i PyMOL. Det er også muligt at bruge kommandoen distance til at finde samme afstande. Distance opretter ligeledes et objekt i objektoversigten, men her udspecificeres et navn til objektet af brugeren. Brugen af distance er som følger:
distance (navn på måling), (første selektion), (anden selektion)Selektionerne gives i en hvilken som helst notation (herunder f.eks. /1efc/B/B/ASN`13/CA eller tilsvarende (resi 13 and chain B and name CA)). Hvis der defineres flere atomer, finder kommandoen samtlige afstande mellem atomer i selektionen. Et tilfældigt eksempel på en afstand mellem to atomer i objektet “1efc” ved navn “d1” kunne således være:
distance d1, /1efc/B/B/ASN\`13/CA, (resi 13 and chain A and name CA)Denne ville altså finde afstanden mellem alfa-carbon i aminosyrerest 13 i kæde A og B.
7.2 Skriv script for GDPNP-visning
Skriv et nyt script, der laver en visning af samme figur som før, men med GDPNP (en analog til GTP) i stedet for GDP og stadigvæk med angivelse af hydrogenbindinger. Hint: Der kan hentes meget inspiration i scriptet fra før.