TØ 18 – Membranpumper
1 Opgave 1. Na/K-pumpen fra skeletmuskulatur
I skeletmuskulatur hos hunde er de ekstra- og intracellulære koncentrationer af Na+ henholdsvis 150 mM og 12 mM, hvor de for K+ er 2.7 mM og 140 mM.
1.1 Beregn fri energi for Na/K-pumpe
Beregn ændringen i fri energi når tre Na+ transporteres ud og to K+ transporteres ind via Na-K-pumpen. Antag at temperaturen er 25°C og at membranpotentialet er -60 mV.
1.2 Vurdér ATP-hydrolysens energi
Ville hydrolyse af et enkelt ATP-molekyle til ADP frigive tilstrækkelig energi til at drive processen? Forklar.
2 Opgave 2. Calciumpumpen
De såkaldte fast twitch-muskelceller fra kaniner indeholder store mængder af den sarco(endo)plasmatiske reticulum calcium ATPase (SERCA).
2.1 Forklar SERCA-modning i ER
Forklar hvorledes modningen af SERCA må forventes at forløbe for at lokalisere pumpen i den korrekte membran
Figur 30.34 i Berg
2.2 Estimér SERCA’s transmembrane helicer
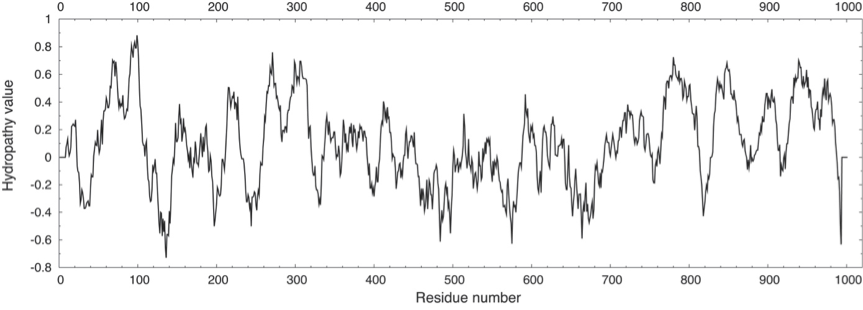
Nedenfor vises et hydropatiplot for SERCA.
Estimér antallet af transmembrane helicer i SERCA og deres omtrentlige placering. Forklar hvordan du når frem til dette.
2.3 Beregn energi for calciumtransport
Koncentrationen af frit calcium i cytoplasma er omkring 0.15 μM, mens den inde i det sarcoplasmiske reticulum ligger på omkring 1.5 mM. Det er calcium ATPasen, der er ansvarlig for at opretholde denne gradient vha. hydrolyse af ATP. Der er derimod i praksis ingen elektrisk potentialeforskel på tværs af SR-membranen.
Beregn forskellen i Gibbs frie energi (i kJ/mol) ved processen hvor to calciumioner transporteres fra cytoplasma til SR, dvs. svarende til én cyklus for SERCA.
3 Opgave 3. Brodys sygdom
Brodys sygdom er en sjælden arvelig sygdom forårsaget af en defekt i ATP2A1-genet, der koder for den almindeligste SERCA1-isoform i det sarcoplasmiske reticulum. Tabellen nedenfor viser en række kinetiske data mål for den calciumstimulerede ATPase-aktivitet i muskelhomogenisater fra kontrolpatienter samt patienter med Brodys sygdom.
| Parameter | Kontrol | Patienter |
|---|---|---|
| Ca2+-ATPase aktivitet (nmol/mg total protein) | 43.9 ± 6.0 | 23.4 ± 3.5 |
| kcat (min-1) | 810 ± 87 | 411 ± 49 |
| Ca2+-ATPase (mg/mg total protein) | 6.12 ± 0.75 | 6.11 ± 0.41 |
| Mængden af SERCA1 i forhold til SERCA totalt set (%) | 82.8 ± 4.6 | 83.4 ± 3.9 |
3.1 Fortolk Brodys sygdoms kinetik
Foreslå en biokemisk fortolkning af de målte data i tabellen. Brug herefter din viden om SERCA’s fysiologiske funktion i muskelfibre til at foreslå hvilke symptomer, patienter med Brodys sygdom kunne tænkes at opleve.
3.2 Forklar bacteriorhodopsin-eksperiment
Et eksperiment blev udført med membranvesikler indeholdende både SERCA og membranproteinet bacteriorhodopsin. ATP blev tilsat til prøven i mørke, hvilket resulterede i målbar ATPase-aktivitet. Efter et stykke tid stoppede denne aktivitet dog selv om der stadig var ATP til stede i opløsningen. Tændte man derimod lyset, genoptoges ATPase-aktiviteten. (Hint: Når calcium flyttes, kotransporterer (antiporterer) SERCA protoner i den anden retning, og det vides at der i gennemsnit flyttes 1.5 proton per calciumion).
Forklar resultaterne i SERCA/bacteriorhodopsin-eksperimentet.
4 Opgave 4. Strukturen af SERCA
Calcium-pumpen fra sarcoplasmisk reticulum (SERCA) blev oprenset af danske forskere fra kaninmuskler, hvorefter strukturer af flere forskellige konformationer blev bestemt vha. røntgenkrystallografi. Download SERCA.pml.
4.1 Identificér transmembrane områder
Identificér først det transmembrane område i SERCA. Hilken ende af strukturen vender ind mod SR og hvilken ende vender mod cytoplasma? Hvorfor skal pumpen vende på denne måde?
4.2 Identificér SERCA-domæner
I oversigtsstrukturen (F1) er SERCAs domæner vist med forskellige farver. Identificér domænerne og angiv kort deres funktion i pumpen.
4.3 Beskriv SERCAs konformationstilstande
Brug F1-F5 til at skifte mellem fem forskellige tilstande. Hvilke tilstande er disse? (Hint: Benyt objektnavnene til højre i vinduet) Forklar kort hvad der sker i mellem hver tilstand.
4.4 Identificér vigtig aminosyre
Tryk F6 for at zoome ind på en vigtig aminosyre for pumpen. Hvilken aminosyre er dette og hvilken rolle spiller den?
4.5 Beskriv aminosyrens modifikation
Aminosyren bliver modificeret som led i enzymets funktion. Da modifikationen er ustabil har man i krystalstrukturen brugt en analog modifikation. Klik på modifikationens atomer og identifér den. Hvilken modifikation repræsenterer analogen og er det en god analog? Hvad interagerer modifikationen med og hvordan påvirker det enzymets struktur?
4.6 Analysér dephosphoryleret tilstand
Tryk endelig F7 for at se aminosyren i en anden tilstand. Hvilken tilstand er dette og hvordan er enzymet forandret?
5 Opgave 5. Na-K-pumpen
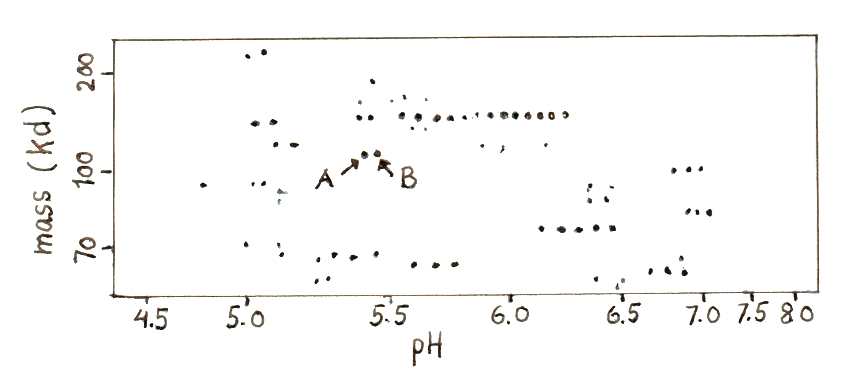
Na+-K+-pumpen (Na+-K+-ATPasen) findes som et integreret membranprotein i pattedyr og dets 1020-aminosyrerester lange sekvens er blevet bestemt ud fra cDNA. I et eksperiment brugte man ekstrakt fra leverceller til en proteomanalyse bestående af todimensionel gelelektroforese efterfulgt af identifikation af enkelte proteinspots ved trypsinering og massespektrometrisk analyse. En del af den todimensionelle gel er vist nedenfor.
Både spots A og B matchede aminosyresekvensen for Na+-K+-ATPasen, men en detaljeret analyse af massespektrene afslørede en interessant forskel: Et fragment med massen 1947.22 Da fra spot A kunne ikke genfindes blandt peptiderne i spot B. Desuden gav spot B et fragment på 1867.89 Da, der meget præcis passer med massen af peptidet NLEAVETLGSTSTICSDK i Na+-K+-ATPasen.
For at identificere fragmentet på 1947.22 Da blev det oprenset og analyseret vha. Edman-degradering, hvilket gav følgende sekvens:
Asn-Leu-Glu-Ala-Val-Glu-Thr-Leu-Gly-Ser-Thr-Ser-Thr-Ile-Cys-Ser-Xaa-Lys. Xaa kunne ikke identificeres.
5.1 Sammenlign spot A og spot B
Hvordan adskiller proteinet i spot A sig fra proteinet i spot B?
5.2 Forklar masseforskel i peptider
Hvad skyldes masseforskellen mellem de fundne, tryptiske fragmenter?
5.3 Identificér modificeret aminosyre
Hvilken aminosyrerest svarer Xaa i spot A til? Opskriv dens kemiske struktur.
5.4 Beskriv phosphoryleringsrestens rolle
Hvilken rolle spiller denne rest i Na+-K+-ATPasens funktion?