TØ 11 – Binding og genkendelse
1 Opgave 1. Indhold af hæmoglobin
Et rødt blodlegeme har et rumfang på 87 µm3 og et gennemsnitligt hæmoglobin (Hb) indhold på 340 mg/ml.
1.1 Beregn Hb-masse per blodlegeme
Hvad er massen af Hb per celle?
1.2 Beregn antal Hb-molekyler per celle
Hvor mange Hb molekyler er der per celle? (tetrameren har en molekylvægt på 65 kDa).
1.3 Beregn krystallinsk pakket Hb-mængde
Hvor meget Hb ville der være per blodlegeme hvis Hb var krystallinsk pakket heri (hver molekyle en terning med 65Å lange sider).
2 Opgave 2. Jern, ilt og hæm
2.1 Beregn jernindhold i menneskekroppen
Hvor meget jern er der i en 70kg voksen person? Antag 70 ml blod per kg kropsvægt og et Hb indhold i blod på 160 mg/ml.
2.2 Beregn \(O_2\)-binding per kg muskel
Menneskemuskel kan indeholde op til 8 g myoglobin (Mb) per kg mens kaskelothvalen har op til 80 g/kg. Hvor meget O2 kan bindes per kg menneske- og hval-muskel når Mb er mættet med ilt?
2.3 Sammenlign iltbinding i Mb og vand
Ilt koncentrationen i vævsvæske ved 37oC er ca. 35 µM. Hvor meget mere (eller mindre) er bundet til Mb i forhold til i vand i hhv menneske og hval?
3 Opgave 3. Kooperativitetsopgave
Fremstilling af teoretiske bindingskurver.
3.1 Udled Hill-ligningen for binding
Vi skal nu udlede og anvende en simpel matematisk funktion til at beskrive kooperativ binding, den såkaldte Hill ligning (ikke noget med bakker men derimod den gode Archibald Hill). Lad os tage udgangspunkt i en simpel binding af substrat S til protein X:
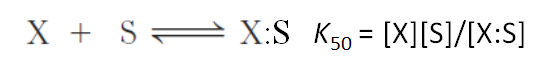
Her gælder at mætningsgraden Y (altså hvor stor en brøkdel af X proteinerne har bundet S) kan skrives som:
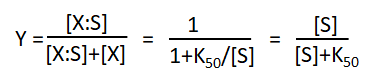
Vi udvider nu denne simple bindingsmodel til at involvere binding af op til n molekyler S per X. Vi antager at hvert S kan binde uafhængigt af de andre S’ere:
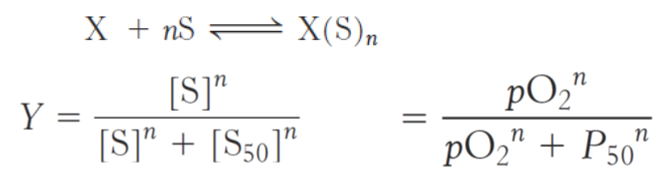
Vis hvordan dette fører til Hill-ligningen:
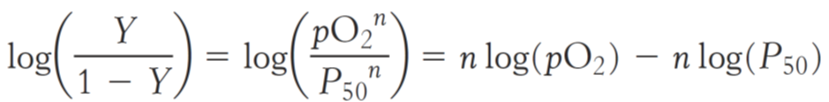
3.2 Plot iltbindingskurve med Hill-ligning
Brug Hill ligningen til at plotte en ilt-bindings kurve for et hypotetisk two-subunit hemoglobin med kooperativitstallet n = 1.8 og p(O2) = 10 torr.
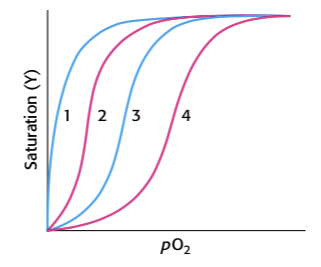
Nedenstående kurve viser flere forskellige ilt-bindingskurver. Kurve 3 svarer til hemoglobin med fysiologiske koncentrationer af CO2 og 2,3-BPG ved pH 7.
3.3 Identificer kurver for bindingsbetingelser
Hvilke kurver svarer til de følgende ændringer i bindingsbetingelserne:
Nedgang i mængden af CO2.
Stigning i koncentrationen af 2,3-BPG.
Stigning i pH.
Tab af kvarternær struktur.
4 Opgave 4. Lampret-fiskens iltbinding
Databehandlings opgave: I denne opgave er det en fordel at bruge Python til databehandling, f.eks. igennem Google Colab
📊 Download lampretfisk_hb_ilt.csv
Lampretfisk er primitive dyr, hvis stamfædre (og ditto mødre!) forgrenede sig væk fra fiskenes stamforældre ca. 400 millioner år siden. Lampretfisk indeholder en hemoglobin (Hb) der er beslægtet med pattedyrs Hb. Der er dog den forskel at lampret Hb er monomert i den ilt-bundne form. Tilførende data for lampret Hb ilt binding kan ses nedenfor eller downloades som .csv ovenfor
p(O2),Y
0.1, 0.006
0.2, 0.0124
0.3, 0.019
0.4, 0.0245
0.5, 0.0307
0.6, 0.038
0.7, 0.043
0.8, 0.0481
0.9, 0.053
1, 0.0591
2, 0.112
3, 0.17
4, 0.227
5, 0.283
7.5, 0.42
10, 0.5
15, 0.64
20, 0.721
30, 0.812
40, 0.865
50, 0.889
60, 0.905
70, 0.917
80, 0.927
90, 0.935
100, 0.941
150, 0.96
200, 0.974.1 Tegn iltbindingskurve for lampret Hb
Lav en ilt-bindings kurve udfra disse data. Ved hvilket ilt tryk er Hb halvt mættet? Udfra kurvens udseende, virker ilt binding til at være kooperativ?
4.2 Lav Hill plot for lampret Hb
Lave et Hill plot udfra disse data. Angiver dette plot kooperativitet? Hvad er Hill koefficienten?
4.3 Forklar kooperativitet via dimermodel
Yderligere studier viser at lampret Hb danner primært dimerer når det ikke er bundet til ilt. Foreslå en model til at forklare den observerede kooperativitet i lampret Hb’s ilt binding.
5 Opgave 5. Allosterispørgsmål
5.1 Analyser effekt af T/R-ratio-mutation
Et allosterisk enzym, som følger MWC (concerted) modellen, har en T/R ratio på 300 i fravær af substratet. Sæt nu at en mutation vender ratioen på hovedet. Hvordan ville denne mutation påvirke forholdet mellem reaktionshastigheden og substratkoncentrationen?
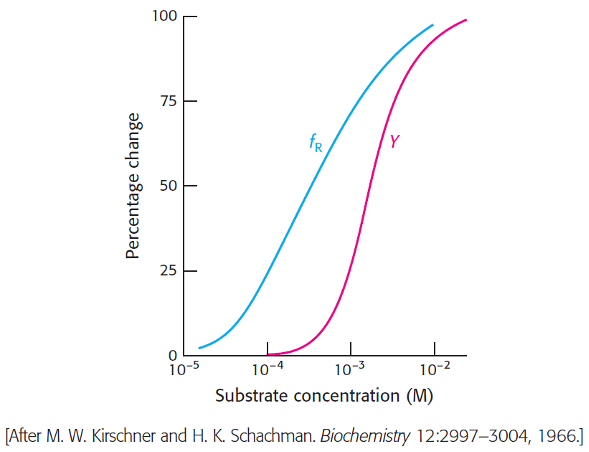
5.2 Vælg model for kooperativ binding
Nedenstående graf viser fraktionen af et allosterisk enzym i R-state (fR) samt fraktionen af aktive sites bundet til substrat (Y) som funktion af substratkoncentration. Hvilken model, MWC eller sekventiel, kan bedst forklare disse resultater?
5.3 Fortolk 430 nm absorptionsændring
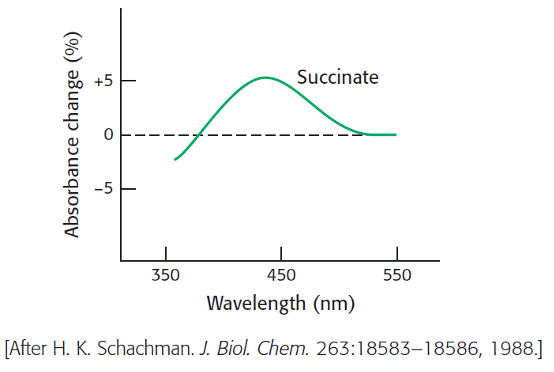
ATCase blev reageret med tetra-nitromethan (TNM) for at danne en farvet nitrotyrosin sidekæde (λmax = 430 nm) i hvert af dens katalytiske peptidkæder. Absorptionen af denne reporter-gruppe afhænger af dens omkringliggende miljø. En essentiel lysin-sidekæde i hvert katalytisk site var endvidere blevet modificeret for at blokere binding af substrat til de aktive site. Katalytiske trimerer blev herefter blevet dannet ved at blande monomerer af dette dobbelt modificerede enzym og det native enzym for at danne hybridkomplekser. Absorptionen af nitrotyrosin sidekæden blev til sidst målt ved titrering af substratanalogen succinate som vist i figuren nedenfor:
Hvad er betydningen af ændringen i 430 nm signalet?
5.4 Analyser ATP og CTP’s effekt på ATCase
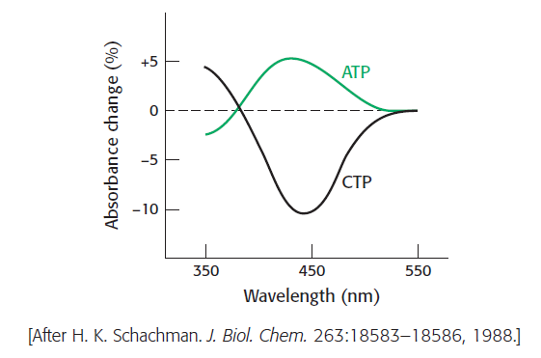
En anden ATCase-hybrid blev lavet til at undersøge effekt af allosteriske aktivatorer og inhibitorer. Almindelige regulatoriske subunits var blandet med nitrotyrosin-indeholdende katalytiske subunits. Titrering af ATP i fravær af substrat øgede absorbansen ved 430 nm, på samme måde som succinate i forrige spørgsmål. Det modsatte observerede man for CTP, hvor titrering af stoffet i fravær af substrate forårsagede et fald i 430 nm absorption:
Hvad er betydningen af disse ændringer i absorbtionen af reporter-sidekæderne?
6 Opgave 6. PyMOL API introduktion (OPTIONAL)
PyMOL-scripting opgave: I denne opgave skal i lære at bruge PyMOLs Application Programming Interface (API) til at skrive jeres egne udvidelser til PyMOL.
Denne opgave er ment som supplement til PyMOL video 6, der handler om brugen af PyMOLs API til at lave PyMOL-udvidelser. Det er derfor en god ide at se den video inden man giver sig i kast med denne opgave.
HUSK:
Start din Python-fil med from pymol import cmd
Før du definerer funktionen med def skrives
@cmd.extendHvis du opretter variable i din funktion, så husk at lave dem inden i et “SPACE” (en dictionary), så du ikke gemmer variable i PyMOL environment. Eks:
my_space={"ny_liste":[ ], "ny_variabel": 22}
Skriv en ny funktion til PyMOL, count_amino_acid(amino_acid), der tæller, hvor mange af en bestemt aminosyre, der er i en selektion og printer dette til konsollen.
Brug cmd.iterate() til at lave en liste over dem, sørg for at der ikke er duplikater i listen og find længden på listen.